国家药品集采近期的两项政策动向引起关注。
8月18日,国家医保局披露2025年全国医疗保障工作年中座谈会的相关情况。在赋能医药产业创新方面,国家医保局明确提出探索开展集采协议期满后全国统一接续采购,降低企业逐省投标成本。在业内看来,这项政策的核心目的是回应产业痛点,解决地方分散续约导致的规则碎片化、企业重复投标成本高等问题。
在优化制度设计的同时,国家层面也在强化质量监管。8月15日,国家组织药品联合采购办公室发布“关于取消江西璟瑞药业有限公司碳酸氢钠林格注射液中选资格并将该企业列入违规名单的公告”。根据公告,作为上市许可持有人,江西璟瑞药业有限公司在确认与验证方面存在缺陷。为预防风险,药监部门已采取暂停该企业碳酸氢钠林格注射液生产销售措施。
上述两条动向看似独立,实则紧密关联,体现了国家药品集采制度的重要改革方向,即从“降成本”向“稳供给+提质量”双轨并进转型,这一转变需要企业予以重视。
300+药品年底协议到期
全国统一接续采购正当时
2018年以来,国家层面已经开展了10批药品集采,覆盖435种药品,最新的第十一批国采正处于医疗机构报量阶段。由于第一批国采接近半数的药品于2020年底协议到期,自2021年开始,国采药品逐步进入接续采购阶段。
2021年4月,上海打响了国采药品接续采购的“第一枪”。通过设置最高有效申报价,企业符合报价要求便可入围,再按照“综合评价指标体系”综合评分,得分最高者获得中选资格。从分值设定不难看出,上海高度重视药企的综合实力,此次接续也被业内视为大型药企的竞争博弈。
与上海同期开展国采药品接续采购的还有北京和天津,但两者皆采用“带量联动、双向选择”的规则,企业拟供应价格符合限价要求便可中选。不过,北京对价差较大的药品创新地提出了梯度带量的方式,即与同组平均价格水平相比,差距每增加1倍,约定任务比例减少10%,最多减少50%。
2021年11月,广东牵头开展阿莫西林等45个国采到期药品的13省(区、兵团)联盟接续,这也是首个以省际联盟方式开展的国采药品接续采购。相较其他省份,改革先锋广东设置的方案更为复杂,采用了医疗机构按照厂牌“开标前初报+拟中选后复报”的双轮报量机制,让中选产品在前期集采降价的基础上平均再降27.5%,最高降50%。
同月,国家医保局办公室发布“关于做好国家组织药品集中带量采购协议期满后接续工作的通知”,首次对国采到期药品作出了“分类开展接续”的部署,要求着眼于维护市场和临床用药稳定,综合考量企业和产品的多方面因素,通过询价、竞价、综合评价等方式确定中选企业和中选价格。遵循这一顶层政策设计,各地进行了有益探索。
其中,江苏在采购量分配上有所创新,采取“两步走”方式:先将同品种医疗机构意向采购量的20%作为优先量,分配给同品种价格最低的前50%企业;再将同品种意向采购量的60%作为剩余量,分配给同品种中质优价宜的中选产品,供医疗机构自主选择。河南则在其牵头的省际联盟国采接续中,提出复活机制和价格纠偏举措,释放了“不唯低价论”的信号。
2023年2月,国家医保局办公室发布“关于做好2023年医药集中采购和价格管理工作的通知”,要求规范国采药品协议期满接续工作,指导上海、江苏、河南、广东牵头开展联盟接续采购,鼓励同一品种由多家企业中选,促进价差公允合理,并统一采购周期。自此,国采接续正式进入四大联盟阶段,并持续至今。
从各具特色但规则差异显著的地方探索,到规则接近统一但偏好不同的四大联盟,国采药品接续的路径逐渐清晰。今年年底,超过300个国采药品协议到期,全国统一接续采购政策的提出恰合时宜,规则统一降低制度性成本,同时以柔性机制平衡临床需求与企业参与度,将推动药品集采从“压价”向“稳供、提质、促创新”的系统治理转型。
全生命周期防控
国采药品质量监管利剑高悬
今年4月起,第十批国采中选结果相继在全国落地,但此前已有山西阳和医药技术有限公司的帕拉米韦注射液、四川海梦智森生物制药有限公司的间苯三酚注射液被取消中选资格,原因皆为监管检查中被发现存在生产问题。值得注意的是,这两家企业皆为B证企业。此次遭到重罚的江西璟瑞药业有限公司,再为所有国采投标企业敲响了一记警钟。
碳酸氢钠林格注射液由日本大冢制药原研,为多种电解质成分组成的复方制剂,适用于循环血量和组织间隙液减少时补充、纠正细胞外液,纠正代谢性酸中毒。在第十批国采时,拥有碳酸氢钠林格注射液注册证书的企业多达15家,竞争激烈。最终,江西璟瑞药业有限公司以4.47元/袋的价格第四序位中标,供应河北、上海、贵州、宁夏四个省份(市、自治区)。
作为上市许可持有人,江西璟瑞药业有限公司此番中选的碳酸氢钠林格注射液由回音必集团江西东亚制药有限公司受托生产,此番问题为确认与验证方面存在缺陷。据悉,确认与验证证明的是药品生产质量所有关键硬件(厂房、设施、设备)和软件(生产工艺、操作规程或方法、系统)可以达到预期结果,范围极广且直指核心,重要程度不言而喻。
根据国家药监局发布的《药品委托生产质量协议指南(2020年版)》,受托双方签订的质量协议应当规定只有在受托方完成必要的确认和验证(包括厂房设施、设备和公用系统等)并达到预期结果时,才能进行产品的生产工艺验证。受托方工艺验证和清洁验证的方案和报告必须经双方审核批准。
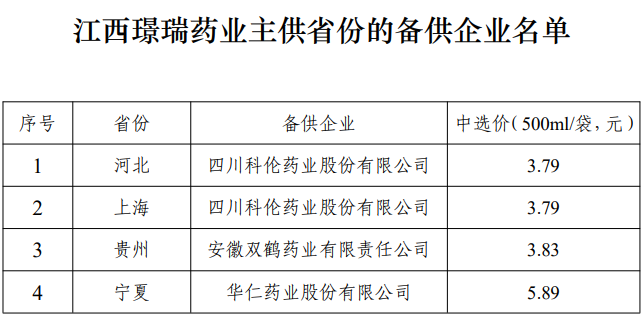
江西璟瑞药业有限公司具体存在的缺陷后续还有待披露,但其因此付出的代价可谓惨痛。除了被取消碳酸氢钠林格注射液中选资格,江西璟瑞药业有限公司还被列入“违规名单”,2025年8月15日至2027年2月14日暂停参与国采活动的申报资格。江西璟瑞药业有限公司被罚后,科伦药业、双鹤药业、华仁药业三家备供企业替补成为主供企业。
值得一提的是,截至目前,国家组织药品联合采购办公室发布过11条国采相关处罚公告,但首次在江西璟瑞药业有限公司的通报中使用了“为预防风险”这一关键字眼,值得玩味。
事实上,药监部门近年来已多次发文加强药品上市许可持有人委托生产监管,要求各省级药监部门加强持有人关键岗位人员的培训和考核,督促持有人持续提升质量管理水平和持续合规能力。日前,安徽还出台《安徽省委托生产药品上市许可持有人关键岗位人员管理办法(试行)》,明确持有人的企业负责人、生产负责人、质量负责人、质量受权人、药物警戒负责人等人员为关键岗位人员,并对其有关履职条件和具体工作职责做出具体要求。
业界普遍认为,全国统一接续采购旨在通过制度优化降低合规企业成本,而严格清退违规企业则是净化竞争环境,两者共同推动集采从降价导向转向质量、成本、供应的三重平衡。未来,随着医保直接结算、按病种付费3.0版等配套措施落地,集采将更深度协同“三医联动”,成为我国医改的核心引擎。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx