中国Biotech企业不懈努力,终于彻底带火了PD-1/VEGF双抗赛道!
日前,普米斯生物技术公司(简称“普米斯”)宣布与BioNTech SE(简称“BioNTech”)达成股权收购协议。根据协议条款,BioNTech将以8亿美元预付款收购普米斯100%已发行股本(可根据惯例对收购价格进行调整),支付方式主要为现金和部分美国存托股份(ADS)。此外,BioNTech将在普米斯达到双方约定的里程碑条件时,额外支付最高 1.5 亿美元的里程碑付款。该交易预计于 2025 年第一季度完成,具体取决于按惯例完成交割条件和监管部门的批准。
无独有偶,另一家“明星”Biotech企业礼新医药,其核心产品LM-299也得到了跨国巨头抛出的橄榄枝。默沙东与礼新医药近期宣布,默沙东已协议获得礼新医药新型在研PD-1/VEGF双特异性抗体LM-299的全球开发、生产和商业化独家许可。

业内观点认为,以PD-1/L1抗体药物为代表的单药治疗和联合治疗方案让肿瘤免疫治疗领域收获了一系列重要突破。然而,除了在全球已经获批的双抗产品之外,随着康方生物PD-1/VEGF双抗通过临床试验数据“头对头”展现出超过帕博利珠单抗(K药)的潜力,宣告了PD-1/VEGF双抗可能在未来抢占更大的市场竞争优势。一大批的国内双抗研制企业在肿瘤免疫治疗领域实现弯道超车,MNC与中国Biotech企业合作成为一个必然选择。
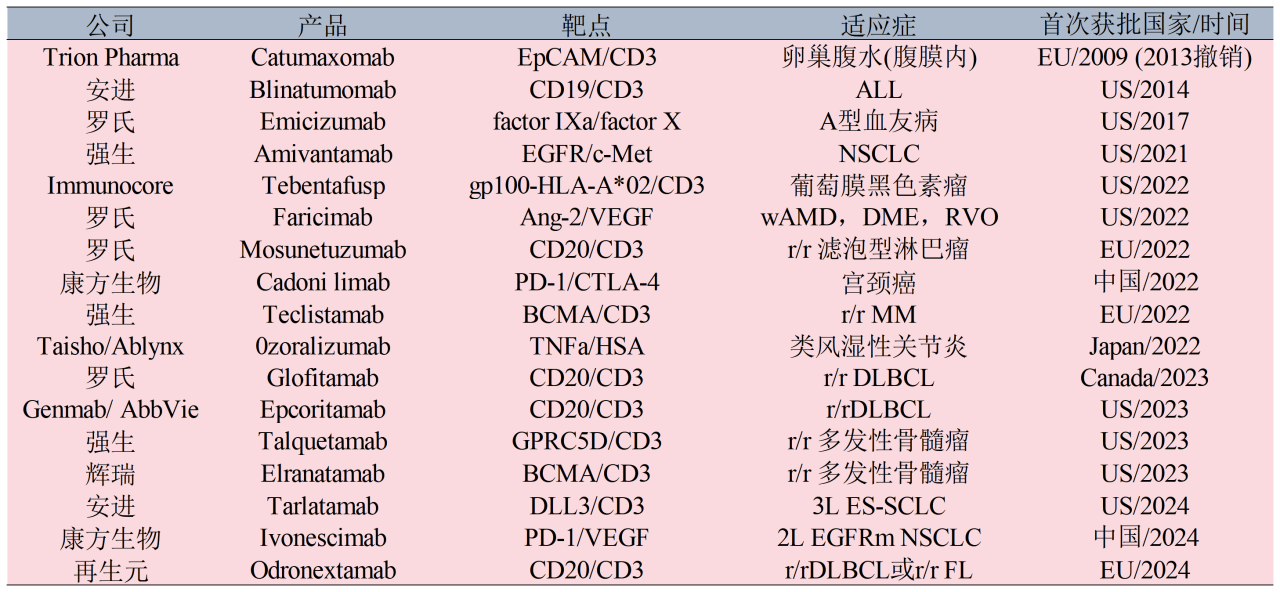
目前全球范围内已获批上市的双抗产品
内卷赛道杀出重围
海外药企积极“抄底”
PD-1/L1一直以来都被誉为“最为内卷的赛道”,PD-1/VEGF双抗展现出的临床突破,似乎有望打破内卷,在这一轮市场竞争中杀出重围。PD-1抑制剂通过阻断PD-1与PD-L1的结合,恢复T细胞的免疫杀伤功能,从而实现对肿瘤的抑制作用。而VEGF抑制剂则通过抑制肿瘤血管的生成,切断肿瘤的营养供应,达到抑制肿瘤生长的目的。将这两个靶点结合起来的PD-1/VEGF双抗药物,理论上能够同时发挥两者的优势,实现更好的抗肿瘤效果。
普米斯成立于2018年,是一家专注于恶性肿瘤和自身免疫疾病领域抗体新药发现和开发的临床阶段生物医药公司。核心产品是其自主研发的抗PD-L1/VEGF双特异性抗体(PM8002/BNT327)。该产品是公司研发管线中进展最快的项目,也是吸引BioNTech进行股权收购的关键因素。
根据普米斯官网介绍,PM8002是新一代基于PD-1免疫调节的双特异性抗体,可同时阻断PD-L1/PD-1以及VEGF信号通路。通过靶向这两个已被临床验证的并具有协同作用的靶点,PM8002有望成为未来肿瘤治疗中的重要的骨架,且可用于联合治疗。
在9月中旬于西班牙巴塞罗那召开的2024年欧洲肿瘤内科学会(ESMO)年会上,吴一龙教授在大会进行口头报告由普米斯生物开展的双特异性抗体PM8002/BNT327联合化疗治疗EGFR突变非小细胞肺癌(NSCLC)的Ⅱ期研究的摘要结果。本次于ESMO大会展示的是一项正在进行的单臂Ⅱ期研究的数据,该研究旨在评估PM8002/BNT327联合化疗治疗EGFR-TKI治疗后进展的EGFR突变的NSCLC患者的疗效和安全性,以及肿瘤PD-L1表达与临床疗效的相关性。
在该研究中,患者接受PM8002/BNT327联合卡铂和培美曲塞Q3W治疗4个周期,随后使用PM8002/BNT327和培美曲塞维持。主要终点是RECIST v1.1评估的客观缓解率(ORR)。结果显示,截至2024年4月12日,64例患者接受了PD-L1 TPS检测,所有患者均可进行安全性和有效性评估。总体ORR为54.7%,DCR为95.3%。在PD-L1 TPS<1%组,ORR为35.7%,DCR为92.9%;在TPS 1%~49%组,ORR为56.5%,DCR为100%;在TPS≥50%组,ORR为92.3%,DCR为92.3%。研究人员认为,PM8002/BNT327联合化疗在EGFR-TKI治疗后进展的EGFR突变NSCLC患者中显示出令人鼓舞的抗肿瘤活性和可接受的耐受性。
此次对普米斯进行股权收购的BioNTech是一家致力于为癌症和其他严重疾病开发创新疗法的新一代免疫疗法公司,主要利用广泛的计算发现和治疗药物平台快速开发新型生物制药产品。其广泛的肿瘤学产品管线包括个体化和通用型mRNA疗法、创新型CAR-T细胞疗法、包括免疫治疗双特异性抗体、肿瘤靶向抗体和抗体毒素偶联物(ADC)在内的大分子药物,以及小分子药物。基于其在mRNA疫苗开发方面的深厚专业知识和内部制造能力,BioNTech及其合作伙伴正在开发用于一系列传染病的多种mRNA候选疫苗,以及多样化的肿瘤产品管线。BioNTech已与多个全球制药公司建立合作,包括复星医药、罗氏、Genevant、Genmab、OncoC4、再生元和辉瑞等。
值得一提的是,在本次股权收购前,普米斯与BioNTech已于 2023 年 11 月就普米斯自主研发的抗PD-L1/VEGF双特异性抗体(PM8002/BNT327)达成全球独家许可与合作协议,该协议授予 BioNTech在除大中华地区以外的全球范围内开发、生产和商业化PM8002/BNT327的权利。或许正是因为看到愈发火热的PD-L1/VEGF双抗所展现出的潜力,BioNTech此次通过直接收购普米斯,进而将PM8002/BNT327完整的全球范围权益收入囊中。
双抗赛道为什么火了?外资企业为何如此看重国内双抗领域药物赛道布局情况?这与前不久康方生物的Ⅲ期临床研究结果不无关系。截至目前,全球已有17款双抗获批上市(包括已经退市的Catumaxomab),其中康方生物凭借卡度尼利单抗和依沃西单抗占据了两个席位。尤其是PD-1/VEGF双抗依沃西单抗,其在Ⅲ期临床研究中表现出显著优于默沙东帕博利珠单抗(K药)的疗效,成为全球首个在单药头对头Ⅲ期临床研究中证明疗效显著优于K药的药物。
在双抗领域国内企业早已展开布局,除了前文介绍的康方生物,还有如信达生物,其与礼来合作开发的IBI-318是一款重组全人源IgG1抗PD-1/PD-L1双特异性抗体,是全球首个进入临床的PD1/PDL1双抗;百济神州与安进合作引进了多款双抗产品,包括Blincyto(CD3×CD19)、AMG701(CD3×BCMA)等6款双抗,同时也有自主研发的双抗管线;恒瑞医药自主研发的SHR-1701(PD-L1/TGFβ双抗)处于临床Ⅲ期,且在多个适应症中展现出良好的治疗效果。
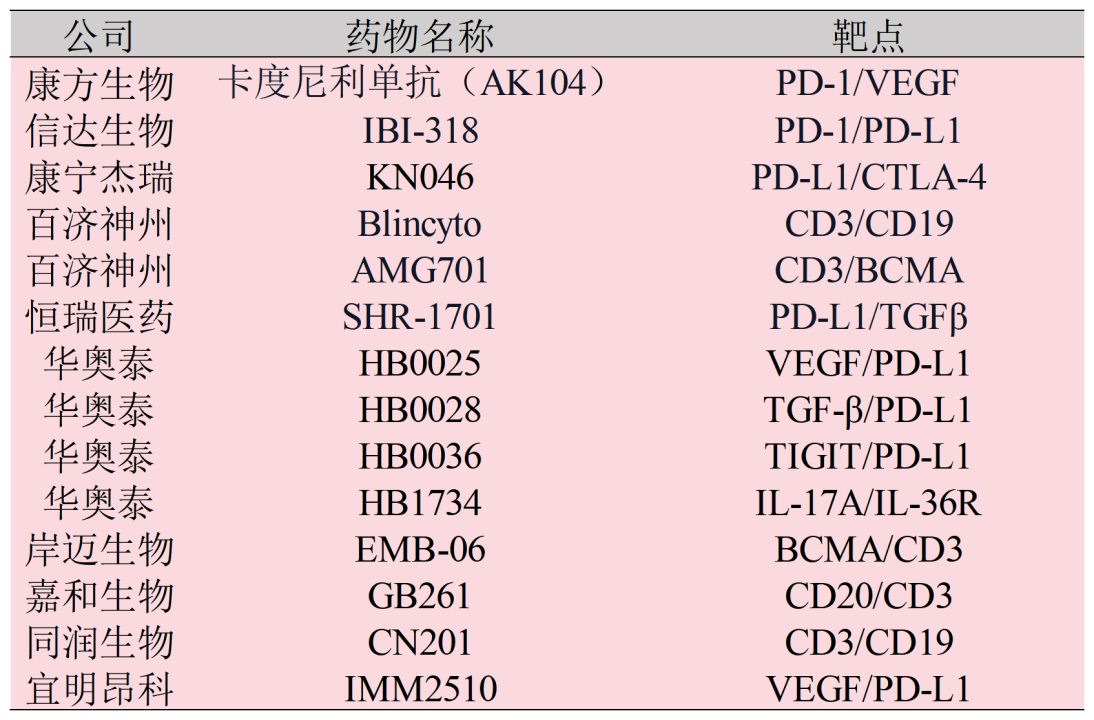
国内部分双抗类产品在研企业
默沙东忍不住了
K药之后下一波浪潮来袭?
全球各大药企开始加大双抗领域围猎力度,力图握住下一场浪潮的船票。
11月14日,默沙东(MSD)与礼新医药宣布,MSD已协议获得礼新医药新型在研PD-1/VEGF双抗LM-299的全球开发、生产和商业化独家许可。根据协议条款,礼新医药已授权MSD LM-299的全球开发、生产和商业化独家许可。礼新医药将获得5.88亿美元的首付款。基于LM-299多项适应证的技术转让、开发、获批和商业化进展,礼新医药还将获得最高27亿美元的里程碑付款。作为一款处在早期研发阶段的产品,LM-299此时被默沙东买断权益,显然传递出不一样的商业气氛。
从默沙东此次收购不难感受到,面对PD-1/VEGF双抗带来的压力,K药已经开始焦虑了。今年9月份,康方生物在第25届世界肺癌大会(WCLC)上发布了HARMONi-2/AK112-303 Ⅲ期临床的详细结果,数据显示依沃西单抗在抗肿瘤效果上显著优于K药。研究表明,依沃西组的PFS为11.14个月,而K药仅为5.82个月,疾病进展或死亡风险减少49%。此外,依沃西在各个亚组中的表现同样卓越,特别是在PD-L1低表达、鳞状NSCLC、伴有脑转移和肝转移的患者中,依沃西单抗同样显著优于K药。同时,依沃西的安全性也得到了验证,与K药相比不良反应发生率相当,且患者的生活质量无明显差异。这一HARMONi-2研究是全球首个成功击败K药的Ⅲ期临床试验,依沃西单抗成为全球首个在单药头对头Ⅲ期临床研究中证明疗效显著优于K药的药物。
事实上,默沙东一直以来全力聚焦K药研发,尤其是K药在单用治疗和联合治疗的开发策略十分清晰,探索也非常积极,围绕PD-1联合VEGF的治疗应用也曾经做出过很大的努力,虽然部分领域如肝癌,PD-1联合VEGF取得了很多成果,但二者联用的方案也并非百试百灵。尤其是在肺癌这个“兵家必争之地”,默沙东此前曾进行过K药联用VEGF抑制剂的研究LEAP-007。LEAP-007研究是一项比较K药+仑伐替尼(一种VEGF抑制剂)与K药单药一线治疗TPS≥1%的NSCLC的临床试验。结果显示,K药+仑伐替尼组的mPFS为6.6个月,而K药单药组的mPFS为4.2个月(HR=0.78,p=0.00624)。尽管在mPFS上取得了获益,但两组在mOS(中位总生存期)上并未显示出显著差异。正因如此,一直以来默沙东对于K药与VEGF联合治疗的方案,兴趣似乎并不积极。
最初,在面对来自康方生物的挑战时,默沙东也没有第一时间采取行动。在康方生物宣布积极数据后不久,默沙东首席医学官Eliav Barr在2024年美国临床肿瘤学会(ASCO)会议上公开表示,依沃西单抗可能是另一种治疗选择,这对患者来说是个好消息。但问题是,默沙东也做过很多K药联用VEGF抑制剂的研究,包括在肺癌中的PFS可以显示阳性,但OS(总生存期)更难做到。随着康方生物HARMONi-2试验数据被公开后,PD-1/VEGF双抗得到的关注迅速提高。
当前,PD-1/VEGF双抗市场爆火,MSD虽然表面强势坚持自己对双药联用的保守倾向,却也难以抵抗战略动作做出诚实的选择。K药虽然是MSD的一个里程碑,为MSD贡献了超四成营收,但随着K药关键专利将于2028年到期,后续的营收利润增速也将放缓,MSD必须减少对K药的营收依赖。MSD需要寻找新的解决方案。
礼新医药是一家年轻的创新药企,2019年由秦莹创立,专注开发ADC和肿瘤免疫学新型生物疗法,目前拥有抗体发现、ADC(抗体偶联药)、双抗三个技术平台。在中国创新药领域,礼新医药是一家在管线授权交易方面战果颇丰的企业。在与MSD达成合作之前,礼新医药已有过多笔出海交易,且买家均是跨国制药巨头。2022年和2023年,礼新医药曾分别将两款在研药物授权给Turning Point(后被百时美施贵宝收购)和阿斯利康,交易总价值分别为11亿美元和6亿美元。此次达成交易的LM-299是一款在研PD-1/VEGF双特异性抗体,其I期临床试验正在中国招募受试患者。
业内观点认为,随着国内药企在双抗治疗药物研发领域逐步取得的成果公布,双抗研究也被国内Biotech企业推上了万众瞩目的舞台,这对于国内外生物制药企业来说无疑是一个巨大的机遇。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx