5月14日,和黄医药发布公告称,其已与恒瑞医药达成合作,启动索凡替尼联合卡瑞利珠单抗用于治疗初治胰腺导管腺癌的2/3期研究。
5月18日,恒瑞医药发布公告称,收到了美国FDA关于卡瑞利珠单抗联合阿帕替尼用于不可切除或转移性肝细胞癌患者的一线治疗的生物制品许可申请的完整回复信。信中回复称会基于企业对生产场地检查缺陷的完整答复进行全面评估,并且由于部分国家的旅行限制,在审查周期内也无法全部完成该项目必需的生物学研究监测计划(BIMO)临床检查。
对于恒瑞的卡瑞利珠单抗,还真是好事多磨,和黄与恒瑞的强强联合,最终又会走向怎样的结局?
出海的不容易
恒瑞医药的卡瑞利珠单抗,已在中国获批9个适应症,是目前获批适应症和覆盖瘤种数量领先的国产PD-1产品,2023年8月其“双艾组合”向FDA提交出的BLA申请获受理,外界对其海外获批上市也曾寄予厚望,如今也充分说明了国产创新药出海的困难程度。
在PD-1领域内,与卡瑞利珠单抗有着经历的,还有信达生物的信迪利单抗,不同的是,未通过批准是因为没有纳入足够的美国患者数据。
生产场地检查缺陷的问题整改其实好解决,也能够解决,毕竟属于药企能够控制的范围内,但在俄罗斯和乌克兰的关键临床试验中心的检查,由于政局缘故,就不在可控范围内了。
参考首个登美国产PD-1的秘诀,FDA对有着同样“缺点”的特瑞普利单抗与替雷利珠单抗,却甚是包容:
2023年10月,一次性批准了特瑞普利单抗的两项适应症,联合顺铂/吉西他滨作为转移性或复发性局部晚期鼻咽癌成人患者的一线治疗;单药治疗既往含铂治疗过程中或治疗后疾病进展的复发性、不可切除或转移性鼻咽癌的成人患者。
2024年3月,替雷利珠单抗获FDA批准,用于单药治疗既往接受过系统化疗(不含PD-1/L1抑制剂)后不可切除或转移性食管鳞状细胞癌(ESCC)的成人患者,产品预计将于2024年下半年在美国上市。
值得注意的是,君实与百济神州PD-1在首项适应症方面并未选患病率更高、市场空间更大的“大癌种”,而是鼻咽癌等小众疾病,这部分适应症美国尚无治疗该类肿瘤的免疫疗法获批,符合美国“未被满足的临床需求”条件,也属于实打实的差异化竞争。
而特瑞普利单抗的登美成功,为其他药企提供了可借鉴经验,替雷利珠单抗的获批,则更加强化了国产创新药出海的信心,思考未来怎样制定能打动美国临床需求的适应症,才能一举撬开FDA的“大门”。
和黄医药的出海梦
和黄医药在肿瘤领域,作为Biotech药企,不仅在港美英三地IPO上市,且自主研发获批了肿瘤药物“替尼三将”,此外,还引进上市了一款EZH2口服抑制剂肿瘤药物--他泽司他。
在“替尼三将”与“他泽司他”的护驾下,和黄医药前几年的亏损业绩并未得到明显的改善,直到2023年,其业绩正式扭亏为盈,据2023年报显示,总收入为8.38亿美元,应占净收益为1.01亿美元。
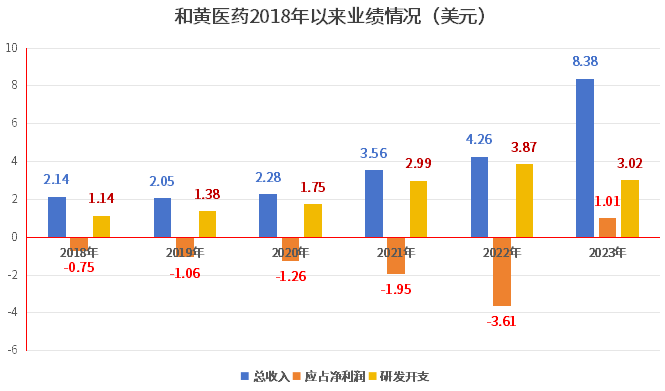
图片来源:根据和黄医药历年年报整理
其2023年扭亏为盈的主要原因,系2023年获FDA批准上市的“呋喹替尼”带来大额的销售业绩。
2023年11月,呋喹替尼获美国FDA批准上市,商品名为FRUZAQLA,用于经治转移性结直肠癌患者,至此,和黄医药终于用自研肿瘤新药开辟了海外新战场,呋喹替尼的销售额也持续走高,2023年销售额为1.23亿美元,同比增长31.12%。
值得一提的是,呋喹替尼美国版(FRUZAQLA)的销售额为1510万美元,这仅仅是2023年11月在美国获批上市后不到2个月的市场表现,此外,和黄医药在2023年还获得武田引进呋喹替尼的4.35亿美元首付款和里程碑付款。
若没有呋喹替尼的出海成功,和黄医药2023年的利润额甚至可能仍是负值。足见出海对于和黄医药业绩的重要性。
至于“替尼三将”中的另外两个,鉴于早些年索凡替尼也曾折戟美国FDA,加之如今呋喹替尼的出海成功,“替尼三将”持续出海已成为必须,索凡替尼要想顺利打开美国市场,进而打开欧洲、日本等其他国家市场,要么补齐国际多中心临床试验短板,要么有新的适应症砝码引起美国FDA的重视。
共同的梦,共同的目标
恒瑞医药的卡瑞利珠单抗,与和黄医药的索凡替尼,都有着登陆美国市场的雄心壮志,然而,都因各自的原因暂时未能如愿以偿。
与PD-1双宿双飞。因索凡替尼有着通过抑制血管生成、阻断肿瘤相关巨噬细胞积累并促进效应T细胞渗透到肿瘤的能力,能有助提升PD-1的抗肿瘤活性,和黄医药正试图通过与PD-1药物联用,拓宽索凡替尼的适应症空间,中国已开展了联合拓益(特瑞普利单抗)治疗9种实体瘤类型的2期研究。
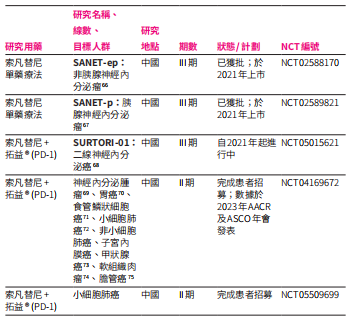
图片来源:和黄医药2023年报
特瑞普利单抗的获批秘诀,是可以复制的经验,选择胰腺导管腺癌作为突破点非常适合,被称为癌王的胰腺癌,患者平均5年存活率低于10%,仅不到20%的转移性胰腺癌患者能夠存活超过一年,而胰腺导管腺癌又占胰腺癌的90%以上,在医疗发达的美国,胰腺癌治疗方案也大同小异。
中国胰腺癌诊疗指南(2022年版)将白蛋白结合型紫杉醇和吉西他滨联用作为多个类型胰腺癌的推荐用药方案之一,而NCCN胰腺癌临床实践指南(2023.V2版)同样如此,尽管在其他推荐方案中新增NALIRIFOX,但也注明“虽然NCCN认可有高级别证据支持NALIRIFOX优于吉西他滨和白蛋白结合型紫杉醇,但应注意到,与FOLFIRINOX相比,似乎并不具有优势,且会增加相当多的费用”。
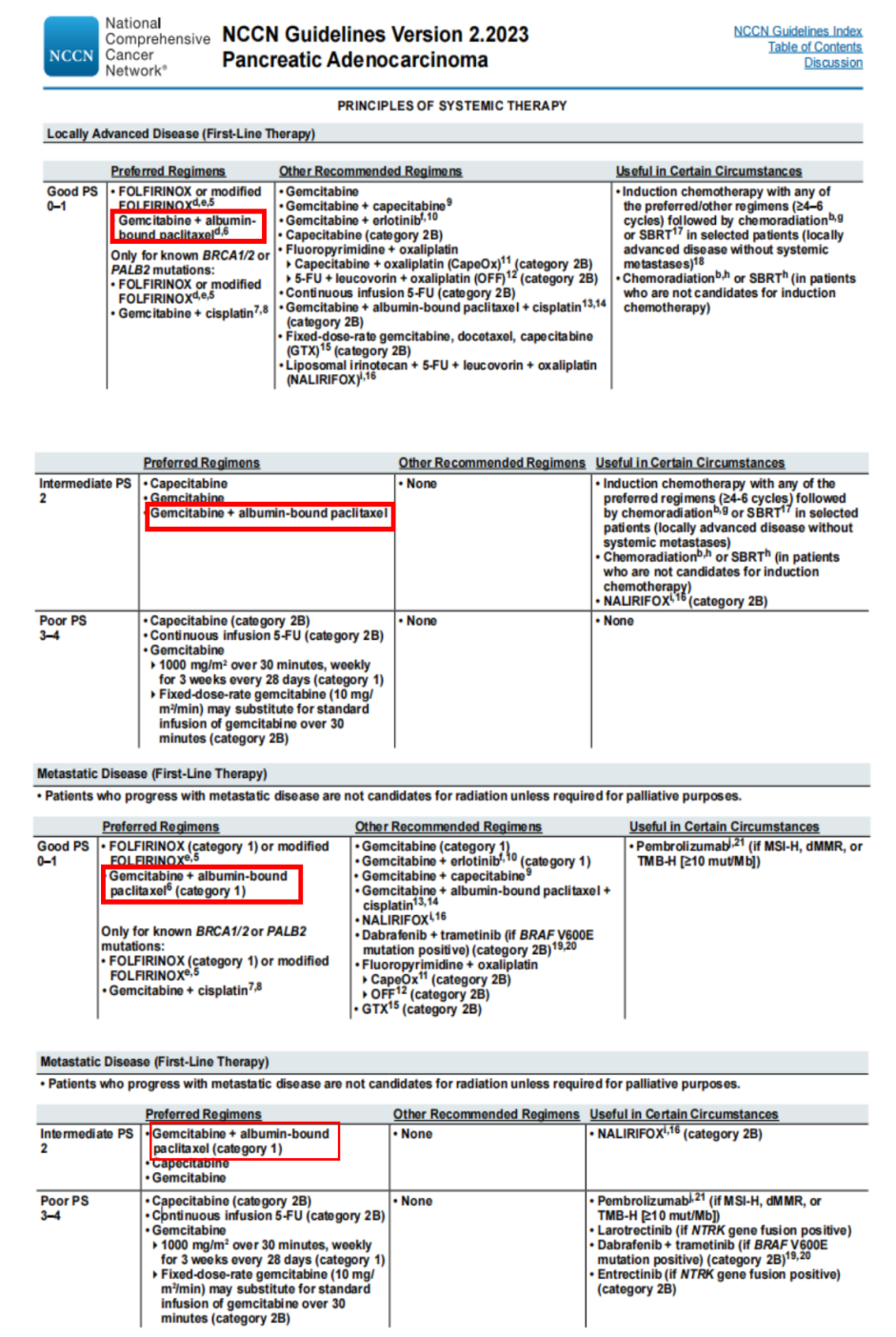
图片来源:NCCN胰腺癌临床实践指南2023.V2版
两强联手,共图霸业。向“癌王”挑战若能成功,将成为索凡替尼被美国FDA重视的砝码,有了突破点,选择并肩作战的“战友”就又是一门学问。
恒瑞医药的卡瑞利珠单抗,已在中国获批9个适应症,成为获批适应症和覆盖瘤种数量领先的国产PD-1产品,其实,和黄医药早就在索凡替尼与其他疗法联合使用的探索性研究中,尝试过与卡瑞利珠单抗联用效果。
据一项使用索凡替尼与卡瑞利珠单抗联合化疗一线治疗胰腺癌的临床试验数据显示,中位PFS及OS分別为9.2个月和15.6个月,索凡替尼仅联合化疗的对照组分別为6.3个月和8.6个月,而单接受吉西他滨和白蛋白结合型紫杉醇联合疗法的中位PFS为5.8个月。
而恒瑞医药也正需要加持卡瑞利珠单抗能够在美获批的含金量,此时,选择与和黄医药合作可谓是明智之举。
据ClinicalTrials.gov查询显示,索凡替尼联合卡瑞利珠单抗的临床试验对比用药方案共3种,分为索凡替尼、卡瑞利珠、白蛋白结合型紫杉醇和吉西他滨的联合疗法、白蛋白结合型紫杉醇和吉西他滨联合疗法,以及索凡替尼、白蛋白结合型紫杉醇和吉西他滨联合疗法。
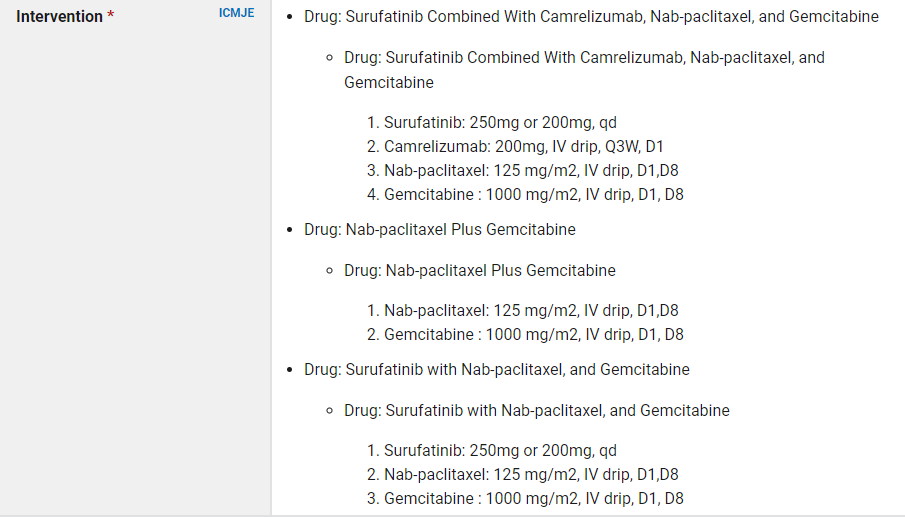
图片来源:ClinicalTrials.gov
和黄医药与恒瑞医药的临床试验目的很明确,就是要替代白蛋白结合型紫杉醇和吉西他滨联合治疗胰腺癌的一线位置。
小 结
好药的研发获批,不能光靠在临床试验上的一味蛮干,重要市场的选择,开发策略的及时调整,往往能为药品的顺利获批上市,以及上市后的市场表现起到决定性作用。
和黄医药及恒瑞医药的强强联合,不仅可助推产品早日在海外获批上市,且快速有效占领市场。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx