华润双鹤 · 巯嘌呤微片
9月29日,据CDE官网公示,华润双鹤巯嘌呤微片申请注册2.2类化药新药获受理。此前,华润双鹤巯嘌呤微片拟纳入优先审评品种,适用于绒毛膜上皮癌,恶性葡萄胎,成人和儿童急性淋巴细胞白血病及急性非淋巴细胞白血病,慢性粒细胞白血病的急变期。

瑞加美生物 · RJMty19注射液
27日,据CDE官网公示,浙江瑞加美生物的RJMty19注射液RJMty19申请临床。注射液是基于人源化CD19-CAR开发的一款现货通用型DNT细胞治疗产品。DNT细胞又称双阴性T细胞,是正常人外周血中表达CD3分子,但不表达CD4和CD8分子的T细胞亚型,比NK细胞具有更强的特异性杀死多种肿瘤细胞的活性和更长的体内持续时间,是一种极有希望用于治疗临床多种肿瘤的现货通用型T细胞药物。
这意味着RJMty19注射液作为全球首款现货通用型CD19-CAR-DNT免疫细胞治疗产品向正式注册临床试验又迈进了一步。
恒瑞医药 · 脯氨酸恒格列净
近日,恒瑞医药收到国家药品监督管理局下发的《受理通知书》,公司提交的1类新药脯氨酸恒格列净(以下简称“恒格列净”)的药品上市许可申请获国家药监局受理,本品拟定新增适应症为:与盐酸二甲双胍和磷酸瑞格列汀联合使用,即在单独使用盐酸二甲双胍血糖控制不佳时,本品可与盐酸二甲双胍和磷酸瑞格列汀联合使用,配合饮食和运动改善成人2型糖尿病患者的血糖控制。
此次提交新增适应症申请的决策基础为1项关键性临床Ⅲ期研究——脯氨酸恒格列净片、磷酸瑞格列汀片、盐酸二甲双胍缓释片三药联合治疗经二甲双胍治疗血糖控制不佳的2型糖尿病受试者的有效性和安全性的III期临床试验(试验编号:SHR3824-SP2086-MET-301)。研究结果表明,恒格列净、瑞格列汀和二甲双胍三药联合治疗方案较两药联合相比,具有更优的降糖疗效。
禾沐基因 · HGI-002注射液
27日,禾沐基因的HGI-002注射液临床试验申请获受理。HGI-002注射液是基于自体造血干细胞的基因治疗,通过提取患者自身的造血干细胞,体外利用慢病毒重新导入具有功能的α-珠蛋白基因,帮助红细胞恢复α-和β-珠蛋白比例及血红蛋白的功能,从而达到帮助地贫患者摆脱输血的效果。HGI-002注射液是禾沐基因继重点开发的第一序列产品HGI-001注射液(治疗β地中海贫血)后的又一重磅研究产品。
亘喜生物 · GC012F注射液
27日,亘喜生物的GC012F注射液临床试验申请获受理。GC012F是一款基于亘喜生物专有的FasTCAR平台技术开发的候选产品,具备“次日完成生产”的优势;该疗法目前正处于多项在中国开展的由临床研究者发起的I期临床试验(IIT),包括此前已经披露的针对复发/难治性多发性骨髓瘤的临床研究。
2021年11月,美国FDA已经授予GC012F孤儿药资格认定。亘喜生物首创性地将BCMA/CD19双靶点CAR-T细胞疗法应用于B-NHL治疗领域,进一步探索GC012F更广阔的临床价值。
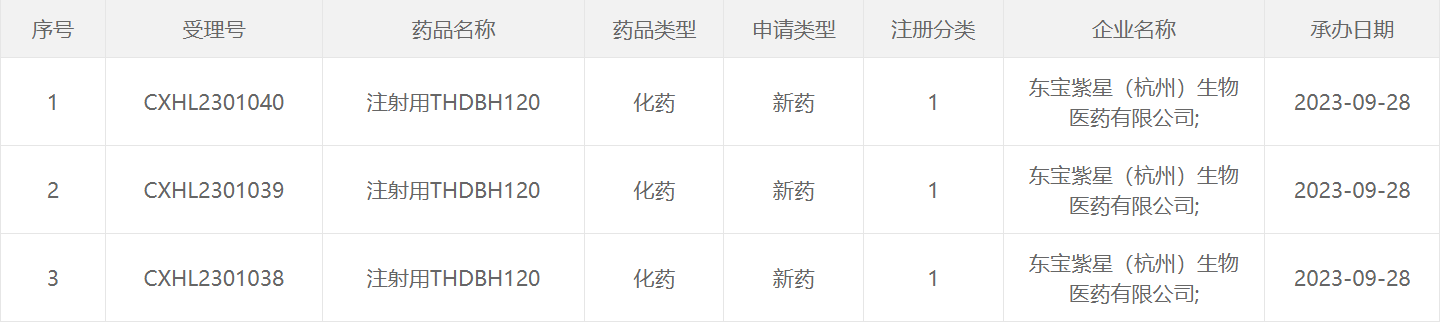
东宝紫星 · 注射用THDBH120
通化东宝全资子公司东宝紫星紧跟全球多肽减肥降糖药主流研发趋势,在GLP-1方面,公司除索马鲁肽外,利拉鲁肽注射液预计将于今年年内获批上市;一类创新药口服小分子GLP-1受体激动剂(THDBH110胶囊)和GLP-1/GIP双受体激动剂(注射用THDBH120)申报临床也均已获得受理。近日,注射用THDBH120的1类化药新药注册已获CDE受理。
逻晟生物 · NB002注射液
逻晟生物自主开发的NB002注射液申请1类治疗用生物制品新药获CDE受理。此前,其用于治疗实体肿瘤的研发管线NB002已顺利通过美国食品药品监督管理局(FDA)审查并同意开展Ⅰ期临床试验。
NB002是一款靶向TIM-3独特表位的单克隆治疗抗体,其不仅显著激活T和NK细胞的活性,增强其对抗肿瘤的能力,更重要的是NB002重建了肿瘤环境中被抑制的天然免疫,恢复DC细胞反应能力,提高髓系细胞抗原递呈功能,整体性解除TIM-3调控的从天然免疫到获得免疫的抑制性作用,有效地增强肿瘤免疫杀伤能力。

【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx