作者:李兴民等(陕西中医学院) ⊙ 编辑:春雪
[摘要]对一项新药临床试验进行回顾性研究发现,知情同意导致反安慰剂效应,严重干扰疗效评估;功能性指标更易受反安慰剂效应的干扰,而客观指标则较为稳定。建议严格选择应用安慰剂的适应症、使用客观指标判定疗效、采用基础治疗与加载试验、谨慎纳入人格缺陷者、暂时隐瞒等应对反安慰剂效应。
新药临床试验须设安慰剂对照。试验前,受试者需要在<知情同意书>上签名,知道他可能接受的是安慰剂治疗,或者是药物治疗。但由于采用盲法取药,被试究竟用了什么药,只有试验结束揭盲后方能得知”。
事先告知患者,使用的可能是试验药,也可能是安慰剂,是有违安慰剂作为临床暗示治疗的本意的。因为这可能导致以下4种情况:
① 给予的是治疗药,患者也认为是治疗药,达到治疗目的;
②给予的是治疗药,患者却怀疑是安慰剂,导致反安慰剂效应;
③给予的是安慰剂,患者也猜测是安慰剂,不产生安慰剂效应;
④ 给予的是安慰剂,患者认为是治疗药,产生安慰剂效应。
第二种猜疑心理在临床药理研究中如果处理不好,就会影响新药疗效的准确判定和评价,使得疗效较好的药物偏离了其确切的疗效而无法上市。
反安慰剂效应是指患者对于治疗方式的疑虑或消极期待而出现的不良反应。患者因怀疑使用了安慰剂而影响治疗的心理现象,属于广义的“反安慰剂效应”范畴。即临床治疗时,对患者施加暗示,并应用安慰剂,但因为操作不当,使患者知道是用“假药”来“欺骗”他,从而对治疗失去信念,结果使病情恶化,即使换为某种治疗药物,患者仍可能认为是在“欺骗”自己,使病情难以很快得到治疗。
反安慰剂效应在国外文献中有较多报道,牛津大学的一项研究证实,反安慰剂效应的确可对大脑的某一特定区域产生作用,并对最终疗效产生消极影响,对大脑中某些区域内神经活动的检测,或可排除安慰剂与反安慰剂效应,客观地衡量出药物的真实效果。
文章依据临床资料,探讨新药临床试验中的反安慰剂效应特点,以及其对疗效评估和不良反应记录的影响,并提出解决路径。
临床试验资料
笔者近年参与了一项治疗单纯性非酒精性脂肪肝的中药复方制剂Ⅱ期临床试验,对照组为安慰剂。疗效性观察指标:症状以右胁胀痛或不适,腹胀、乏力为主(以量化的分值进行评估),影像学检查以CT肝脾比值作判断(0.5<肝/脾CT比值≤0.7者为中度;肝/脾CT比值≤0.5为重度)。
该临床试验疗程为24周,从2008年10月—201 1年l2月在4个中心(均为国家新药临床研究机构)同时进行。结果见表1。
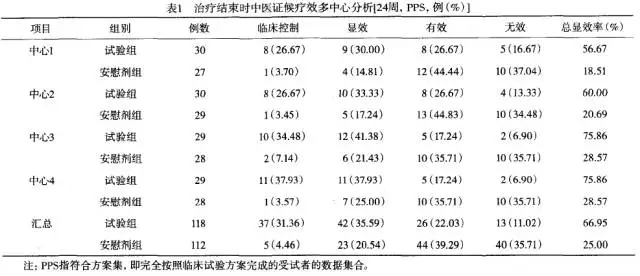
中心1、中心2试验组和安慰剂组,总显效率(临床控制+显效)均明显低于中心3和中心4,且中心1和中心2疗效接近,中心3和中心4疗效接近。
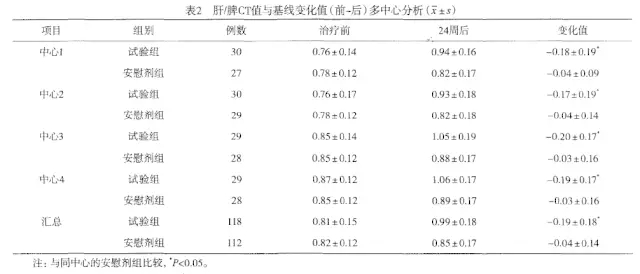
表2数据为治疗前、后肝/睥CT比值的变化结果,两组治疗前肝/脾CT比值比较无统计学意义,治疗前与用药24周后差值(变化值),两组间多中心分析,肝/睥CT比值组间比较有统计学意义(P<0.05),中心间比较无统计学意义。
结论
临床症状疗效观察结果2个中心疗效较好,另2家较差。分析原因发现,疗效好的2个中心的研究者有意模糊处理了<知情同意书>中关于安慰剂部分的内容;其他2个中心则对安慰剂部分作了比较详细的介绍,结果疗效差异较大。因此,可判定中心1、2出现了“反安慰剂效应”。
表2提示试验组优于安慰剂组。可以看出,肝/睥CT比值是“硬指标”,受反安慰剂效应的影响较小。
试验药原为医院制剂,已应用5-6年,对它的不良反应有一定了解。故在<知情同意书>中对可能出现的不良反应做了提示。结果试验组4例(3.33%),安慰剂组3例(2.50%)出现了恶心、腹泻或皮肤瘙痒。其中1例(安慰剂组)因皮肤瘙痒较重退出试验。
另一项对105例癌症患者相关疲劳(cancer related fatigue,CRF)治疗的研究也显示 ,安慰剂组出现失眠(79%)、厌食(53%)、恶心(38%)和烦躁(34%)等不良反应。分析显示,这些反安慰剂效应与对不良反应的提示有关。
建议
应用安慰剂存在许多弊端,对安慰剂的应用国外已有很大争议。以下就新药研究中安慰剂效应和反安慰剂效应所产生的负面影响提出几点应对办法。
1.严格选择应用安慰剂的适应症
应该说不是所有的新药研究都可以应用安慰剂,也不能说功能性疾病可以用,器质性疾病就不可以用。功能性疾病若受暗示过强,又没有一定的实验室或功能性检查的控制,应用安慰剂应该说是有困难的。如失眠、抑郁症、躁狂症等,常可以从安慰剂效应中获得50%的治疗率或缓解率;癔症性精神障碍、强迫症、惊恐障碍等,也可以从安慰剂效应中获得34%左右的疗效;短期精神分裂症可以从安慰剂效应中获得43%左右的疗效。像这类功能性疾病,若没有“硬指标”控制,都应尽量回避选用安慰剂。对有些器质性疾病,如心绞痛,有报告称应用安慰剂可使30%患者症状得到改善;早期糖尿病肾病安慰剂组总有效率达73.33%。
对高血压病(轻中度)短期应用安慰剂是符合伦理的,其次如高血脂症、脂肪肝、慢性支气管炎等,有些患者平常并不用药,新药研究疗效评定又有实验室或功能检查的“硬指标”,是可以应用安慰剂的,但应制订观察内容和应对病变的措施。
2.尽量使用客观指标判定疗效
客观指标是指实验室检查或功能性检查,它不易受心理暗示和情绪支配,作为疗效主要判定标准,在一定程度上可以减少安慰剂效应和反安慰剂效应的不良影响。如高脂血症的新药研发临床试验,疗效判定应以血脂检查为主(血清总胆固醇、甘油三酯、高密度脂蛋白、低密度脂蛋白)。又如骨质疏松症等症状主要是全身无力,且有明显的腰背部疼痛,但对它的疗效判定应以骨密度检测为主,可应用双能x线(DEXA)、双光子(DPA)、单光子(SPA)等仪器进行检测。
又如中轻度Ⅱ型糖尿病(平均血糖≤11.1mmol/L,糖化血红蛋白≤8.5%)临床试验,可以考虑两组同时在基础治疗下,选用安慰剂作对照,它的疗效指标除血糖测定和口服葡萄糖耐量试验(OGTT)外,还应检测糖化血红蛋白。
3.基础治疗与加载试验
“基础治疗”涉及面较宽泛,包括一些生理行为等内容。“加载试验”主要是配合一定药物的叠加应用。这两种配合方法,都有利于减少反安慰剂效应。
基础治疗,如应用中药复方制剂治疗脂肪肝(新药Ⅱ期临床),我们设计的临床试验方案中,试验组和安慰剂组同时配合基础治疗,内容为:
①改变不良生活方式及行为,合理运动,限制饮酒,育龄期妇女严格执行避孕措施,避免试验期间意外怀孕;
②饮食控制方案,患者在试验期间应减少饱和脂肪酸及胆固醇的摄人(如:肥肉、内脏、蛋、煎炸食品、奶油糕点等,摄入瘦肉量<75g/d,摄入禽蛋量<3个/周),摄人充足蛋白质,保证占总热量的20%,碳水化合物占50%-55%,脂类占25%-30%。不饮酒或每周酒精摄人量<40g;
③运动治疗,中等量的有氧运动60min/d,每周至少5d,如以每隔3d增加步行50步,至每天步行至10000-12000步,20-40min/d。这样的基础治疗对试验组和安慰剂组都具有治疗作用,不过试验组的治疗更积极一些而已。
加载试验又称叠加设计。美国FDA<植物药生产指南>(2004版)提出:对于已经建立了有效治疗的严重疾病,建议申请者在初期临床试验中采用叠加法,即将药物与安慰剂对照,分别加用到标准治疗上去,利用阳性药物治疗组再加安慰剂对照(例如三臂试验)。
若在<知情同意书>中,告知受试者本试验是在有效治疗的标准下,加入试验药物和安慰剂的,意在观察加与不加哪一个疗效更好,这样就使受试者的治愈信念转移到了标准治疗上,对试验药和安慰剂就不再特别关注,也就减少了反安慰剂效应。
4.谨慎纳入人格缺陷者
轻度心理问题或人格障碍在人群中高发,这使新药临床研究产生偏倚的可能性很大,应引起重视。易受到暗示的主要是癔病型人格障碍,其受暗示性和依赖性强;其次是强迫型人格障碍,过分注意安全感易导致怀疑和过分谨慎;另外偏执型人格障碍,也敏感多疑。他们会过分警觉在试验中应用安慰剂,从而出现较强的安慰剂效应和反安慰剂效应。
在纳入受试者时应同时请心理医生参加,必要时作“人格测试”,以排除人格障碍或存在某些心理问题的受试者。
5.暂时隐瞒
国外有学者提出“语境化的知情同意”,即采用“模糊处理”的务实态度,消除反安慰剂效应。
美国心理协会提出以下2种情形可以“隐瞒”治疗手段 :
① 该研究有显著的社会和科学价值;
②不“隐瞒”的手段无法达到试验目的。
但要求,对于能够影响受试者参与试验意愿方面,不得隐瞒;研究结束时,应当向受试者解释清楚“隐瞒”的原因。
美国心理协会还提出了“经受试者认可的隐瞒”,即告知受试者,为达到理想的试验效果,试验过程会隐瞒部分技术手段,绝对不是影响参与试验意愿的方面,在试验结束后会将隐瞒的部分向受试者解释清楚。
<药品注册管理办法>指出:Ⅱ期临床试验为治疗作用初步评价阶段,其目的是初步评价药物对目标适应症患者的治疗作用和安全性,也包括为Ⅲ期临床试验研究设计和给药剂量方案的确定提供依据。因而,在此环节采用“模糊处理”有其合理性。
我国药物临床试验质量管理规范(GCP)尚不允许对患者隐瞒使用安慰剂的实情,使很多时候无法科学使用安慰剂,导致难以客观评价药物真实疗效,也给药审工作带来—定的困难。“暂时隐瞒”可研究借鉴。
对于新药临床研究中的安慰剂使用,我国还没有具体规定的正式文件或指导意见。因而,在使用安慰剂时盲目性和随意性明显,对如何解决安慰剂效应和反安慰剂效应造成的评估偏倚也缺乏研究。科学利用安慰剂,才能使临床试验更加科学合理。
本文摘自:<中华中医药杂志>,2015年,2月第2期
======联系我们=========
天之力医药(微信号:bjtianzhili)专注于医药产品力提升。
回复数字“2”可查看历史推送文章。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx