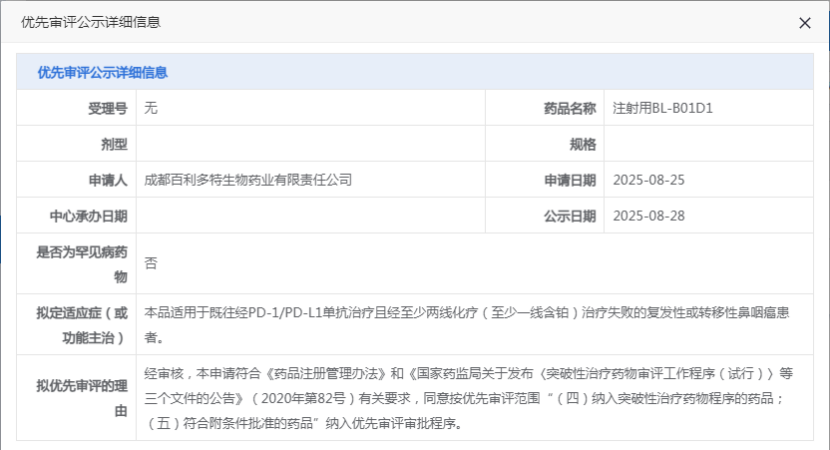
8月28日,CDE官网显示,百利天恒旗下百利多特生物申报的注射用BL-B01D1(伦康依隆妥单抗)拟纳入优先审评,用于既往经PD-1/PD-L1单抗治疗且经至少两线化疗(至少一线含铂)治疗失败的复发性或转移性鼻咽癌患者。
伦康依隆妥单抗是百利天恒自主研发的全球首创(First-in-class)、新概念(New concept)且唯一进入Ⅲ期临床阶段的EGFR/HER3双抗ADC,其小分子毒素部分为百利天恒自主研发的喜树碱衍生物ED04。今年7月,百利天恒宣布伦康依隆妥单抗治疗鼻咽癌的Ⅲ期临床试验BL-B01D1-303在期中分析达到主要终点,成为全球首个完成Ⅲ期研究的双抗ADC。
百利天恒曾在ASCO 2023大会上公布伦康依隆妥单抗治疗鼻咽癌的I期研究数据。结果显示,24例鼻咽癌患者接受治疗后,ORR为45.8%,疾病控制率(DCR)为100%。2023年12月。BMS与百利天恒达成协议,以84亿美元的总交易额获得该药物在中国和美国以外地区的独家开发和商业化权益以及在美国的合作开发和商业化权益。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx