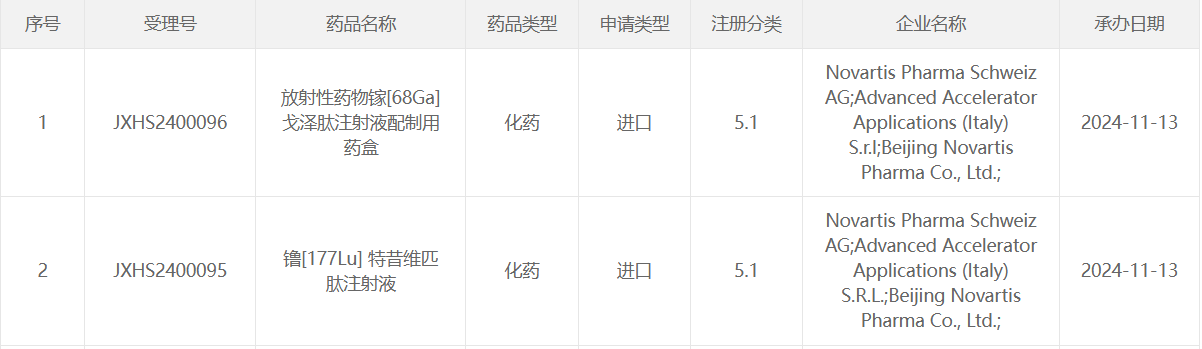
今日,诺华的镥 [177Lu] 特昔维匹肽上市申请获 CDE 受理。
此前该药已被 CDE 纳入优先审评,适用于治疗前列腺特异性膜抗原(PSMA)阳性转移性去势抵抗性前列腺癌(mCRPC) 、已接受雄激素受体通路抑制和紫杉类化疗的成年患者。该药是 FDA 批准的首个针对去势抵抗性前列腺癌患者的靶向放射性配体疗法,本次是在国内首次报上市。
镥 [177Lu] 特昔维匹肽(177Lu-PSMA-617)是一款 PSMA 靶向放射性配体疗法,其将 PSMA-617 与发射β射线的 177Lu 连接在一起,与表达 PSMA 的前列腺癌细胞结合后,177Lu 释放的辐射能量会辐射并杀死肿瘤细胞。
2022 年 3 月,镥 [177Lu] 特昔维匹肽被 FDA 批准用于治疗接受过雄激素受体(AR)抑制剂和紫杉烷类化疗治疗的 PSMA 阳性成人转移性去势抵抗性前列腺癌(mCRPC),商品名为 Pluvicto。
Pluvicto 是 FDA 批准的首款用于治疗这类 mCRPC 患者的靶向放射配体疗法,其获批是基于关键性 III 期临床试验 VISION 的积极结果。
Pluvicto 上市后第二年(2023 年)销售额就达到 9.8 亿美元,同比增速高达 263%。诺华最新三季报显示,2024 年前三季度,销售额已达 10.41 亿美元。以放射配体疗法为代表的核药是诺华重金布局的领域。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx