在经历长达数年的专利战后,阿斯利康1.07亿美元抗癌专利药物赔偿判决迎来反转。
日前,美国特拉华州联邦法官驳回了陪审团就“阿斯利康奥希替尼(Tagrisso)因侵犯辉瑞的抗癌药物奈拉替尼(Nerlynx)专利而赔偿1.07亿美元”的裁决,美国地方法院法官认为辉瑞指控阿斯利康畅销肺癌药物Tagrisso侵犯其两项专利无效。

2021年,辉瑞起诉阿斯利康,指控后者的奥希替尼侵犯了其旗下乳腺癌药物奈拉替尼相关的专利。财报显示,奥希替尼在2023年为阿斯利康带来近58亿美元的收入。业内认为,若最终仍判定构成侵权,阿斯利康势必将失去奥希替尼的产品优势,并还要支付相应金额的赔偿金。
药物研发是一个高投资、高风险、长时间的过程,专利为医药公司提供了一定期限的市场独占权,以补偿其在研发过程中的投入,并激励持续的创新。专利不仅是技术创新的保护伞,也是商业竞争中的重要武器。两大制药巨头在重磅药物上发生专利纠纷无可厚非,但如今胜利的天平已经向着阿斯利康的方向倾斜。
 辉瑞指控被判无效阿斯利康保住业绩支柱
辉瑞指控被判无效阿斯利康保住业绩支柱据了解,辉瑞在2009年以680亿美元收购惠氏后,获得了为治疗HER2阳性乳腺癌而开发的激酶抑制剂奈拉替尼。2011年,Puma Biotechnology从辉瑞获得了奈拉替尼的授权,并全权负责该药物的全球开发和商业化。
该案件中的原告是辉瑞子公司惠氏和Puma Biotechnology,二者在2021年首次起诉阿斯利康,指控阿斯利康的奥希替尼侵犯了两项关键专利。第一项专利被称为“314专利”,涉及用一种与蛋白质半胱氨酸773残基共价结合的表皮生长因子受体阻断剂治疗对吉非替尼(gefitinib)和/或厄洛替尼(erlotinib)耐药的非小细胞肺癌(NSCLC)患者的方法。
另一项是侵犯了惠氏的“162专利”,该专利保护使用这些不可逆抑制剂治疗对吉非替尼或厄洛替尼耐药的、携带表皮生长因子受体(EGFR)蛋白上特定 T790M 突变的 NSCLC 患者。
惠氏的奈拉替尼均采用了这两项专利技术。奈拉替尼是一种激酶抑制剂,与阿斯利康的奥希替尼类似,能与表皮生长因子受体不可逆地结合。奈拉替尼的适应症为 HER2 阳性乳腺癌。
2024年5月,美国特拉华州联邦陪审团一致认定阿斯利康侵犯了惠氏所谓的“312专利”中的三项权利要求和“162专利”中的一项权利要求。这些侵权行为同时适用于 Tagrisso 的二线和一线辅助治疗。陪审团支持了辉瑞公司的主张,并判定阿斯利康给予该公司1.075亿美元的赔偿金。但与此同时,陪审团并没有发现阿斯利康故意侵犯惠氏专利的证据。
但在这次最新的裁决中,当地法官认为辉瑞制药指控阿斯利康奥希替尼侵犯其两项专利无效。因为这些专利缺乏对其发明的有效书面描述,并且该领域的普通科学家无法重新创造它们。
事实上,在医药领域企业之间的专利纠纷屡见不鲜。除了与阿斯利康的专利纠纷外,在奈拉替尼这款重磅药物上,辉瑞与仿制药企业近年来也发生了多起专利链接行政裁决和诉讼。
2020年,奈拉替尼获批在中国上市,用于治疗HER2阳性的早期乳腺癌成年患者,在接受含曲妥珠单抗辅助治疗之后的强化辅助治疗。公开资料显示,奈拉替尼在国内等级医院和零售市场销量呈现出稳步上升的趋势,仅在2022年就达到了1.14亿元市场规模。在2023年上半年,奈拉替尼在等级医院市场销售额继续保持亮眼的增长趋势,达到了6900万元。
Puma Biotechnology在中国上市药品专利信息登记平台上共登记了4件授权专利,其中前两件专利CN103893140B(专利1)、CN102724970B(专利2)是涉及化学药品含活性成分的药物组合物专利,后两件专利CN101918390B(专利3)、CN106822127B(专利4)涉及化学药品医药用途专利。

但在2023年9月,上海创诺制药的马来酸奈拉替尼片获批上市,用于HER2阳性早期乳腺癌成年患者,在接受含曲妥珠单抗辅助治疗之后的强化辅助治疗,成为国内获批上市的首款马来酸奈拉替尼片仿制药。值得注意的是,创诺制药在马来酸奈拉替尼片的上市审批过程中成功地使用了4.2类专利声明,避免了原研厂商对其上市审批进程的干扰。
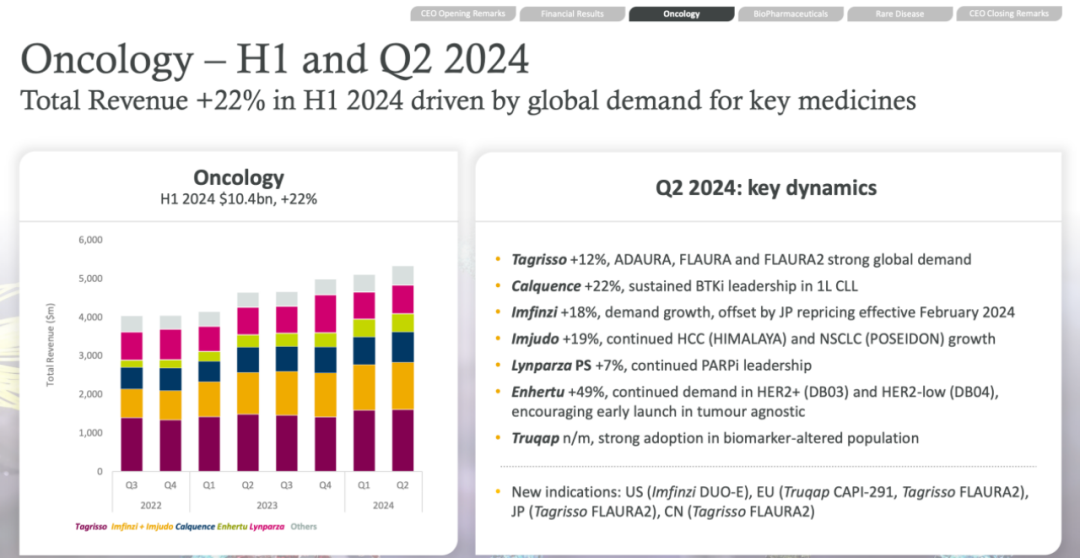
作为阿斯利康的业绩支柱,奥希替尼凭借其于EGFR突变NSCLC二线治疗、一线治疗以及术后辅助治疗的层层递进,业绩一路保持稳健增长,2023年销售额为57.99亿美元。在全球竞争激烈的情况下,奥希替尼在2024年上半年营收同比增长13%至32.02亿美元,全年有望突破60亿美元。
业内普遍认为,专利侵权案件的结果对医药企业的未来发展至关重要。如果阿斯利康最终被判定构成侵权,不仅可能失去奥希替尼的市场独占权,从而面临来自仿制药的激烈竞争,还可能需要支付1.07亿美元的巨额赔偿金。不过从目前来看,阿斯利康在这场专利纠纷中已赢得更多支持,辉瑞后续将如何反击有待观察。
 众多挑战者在路上奥希替尼考验不容小觑
众多挑战者在路上奥希替尼考验不容小觑尽管法院作出了有利于阿斯利康的裁决,取消了辉瑞公司因专利侵权案获得的1.07亿美元赔偿金,不过奥希替尼作为一种靶向治疗药物,在非小细胞肺癌(NSCLC)治疗领域占据重要地位,市场潜力巨大的同时也吸引了众多竞争者的进入。
作为首个上市的第三代EGFR-TKI,奥希替尼的临床研发及上市过程可谓势如破竹,一路高光。2015年11月13日,奥希替尼在美国获批上市,成为第一个在临床上获得应用的第三代EGFR-TKIs。2017年3月,奥希替尼首次获批进入国内市场,从受理(2016年9月)到上市申请批准(2017年3月),仅用了7个月。
奥希替尼在国内上市第二年(2018年)即通过谈判纳入全国医保乙类目录,2020年成功续签,一线及二线适应症全部纳入医保。据悉,在正在开展的2024全国医保目录调整中,其新增适应症(联合化疗一线治疗晚期或转移性EGFR突变肺癌患者)已通过形式审查。
进入医保后,奥希替尼持续放量,米内网数据显示,近年来甲磺酸奥希替尼片在中国三大终端六大市场的销售额稳步增长,2022年突破50亿元,同比增长约6%。
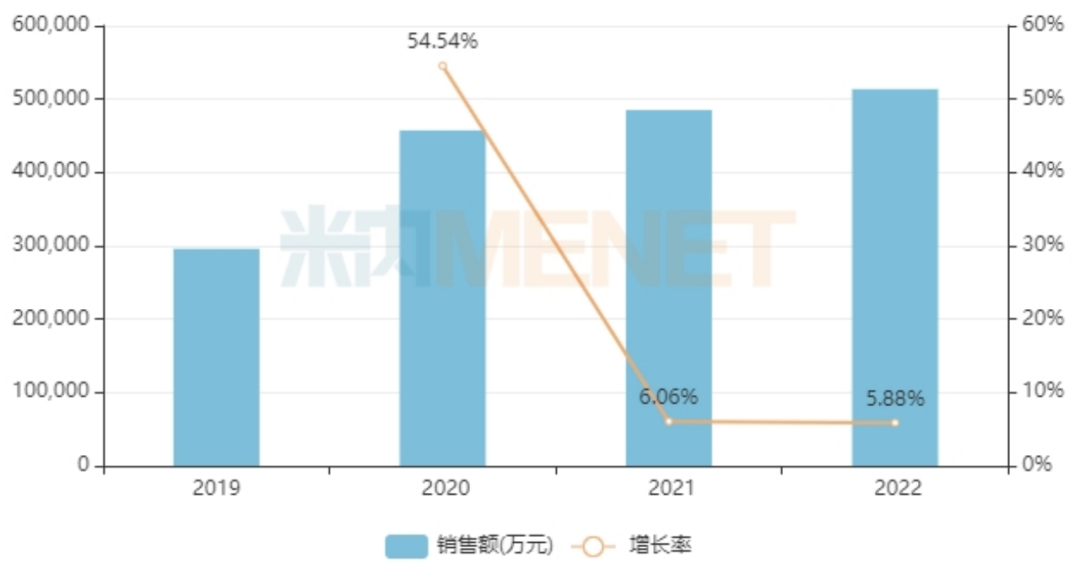
甲磺酸奥希替尼片在中国销售情况
值得一提的是,奥希替尼国内化合物专利CN103702990将于2032年7月到期。业内有观点认为,奥希替尼是近年来上市的进口抗癌药中名气最大、对中国患者影响最大的药物之一。不过,越是畅销的重磅品种,就越容易被竞争者锁定。从产品数量上看,第三代EGFR-TKIs竞争十分激烈,全球已获批产品高达7款,其中国内已批准6款。
面对奥希替尼所占领的庞大市场,有不少药企开展布局,其中江苏万邦生化医药集团布局仿制药,其产品于2020年8月完成BE试验,2021年5月递交上市申请,2023年10月顺利获批生产,拿下国内首仿+首家过评。
除了仿制药的布局,国产原研药物也在这一领域取得了显著进展。阿美替尼是首个国产原研的第三代EGFR-TKI,由江苏豪森药业开发,于2020年3月正式获批上市。2023年,阿美替尼销售额达35亿元。紧接着,艾力斯医药的伏美替尼于2021年3月3日获批上市,成为国内第二个国产第三代EGFR-TKI药物。2023年,艾力斯的伏美替尼销售额达19.8亿元。
此外,目前国内还有多款在研第三代EGFR-TKIs,其中limertinib(奥赛康)、兰泽替尼(强生)已在国内申请上市。此外,TY-9591(同源康医药)、FHND-9041(正大丰海)、艾维替尼(艾森医药)等进入3期临床试验阶段。
肺癌是全球第一大癌,EGFR是一种常见的肺癌驱动基因。全球针对EGFR靶点不仅开发了小分子化药,还开出了单抗、双抗等药物类型。其中小分子EGFR-TKIs是NSCLC治疗领域非常重要的一类靶向药,目前已取得巨大成功,且经历了三代更迭。
据Frost&Sullivan预计,2021年我国EGFR-TKIs市场规模达130亿元,预计2025年和2030年有望分别达到285亿元和522亿元。鉴于目前国内EGFR-TKIs的市场格局,尤其是第三代EGFR-TKIs,未来该领域的竞争必将更加白热化。
目前,奥希替尼凭借其显著的疗效和先发优势,已经成为市场的领导者。然而,随着越来越多的药企加入这一领域的竞争中,未来第三代EGFR-TKIs市场的竞争格局预计将变得更加激烈。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx