在制药行业,专利不仅是保护创新的盾牌,也是市场竞争的利剑。
此前,美国FDA批准了MSN Laboratories的Entresto仿制药,这一决定对诺华公司的原研药市场构成了挑战。诺华为了维护其心力衰竭药物Entresto的市场独占权,于7月31日在华盛顿特区的联邦法院对FDA提起诉讼。
Entresto(诺欣妥,沙库巴曲缬沙坦钠片)是心血管领域的明星产品,最早于2015年7月在美国获得FDA批准上市,用于治疗射血分数降低的慢性心力衰竭(HFrEF)成人患者,以降低心血管死亡和心衰住院风险。2017年,诺欣妥在中国上市,用于治疗心衰,并且已被纳入国家医保目录。2021年6月,诺欣妥在中国获批用于治疗原发性高血压。
作为一款心衰和高血压治疗领域的突破性创新药,诺欣妥的销售额在过去几年中表现出色,迅速成为推动诺华销售增长的“重磅炸弹”产品。2023年的销售额达到了60.35亿美元,同比增长31%,成为诺华最畅销的产品;在2023年的财务报告中,诺华对诺欣妥的市场潜力持续看好,预测其销售峰值有望达到70亿美元。
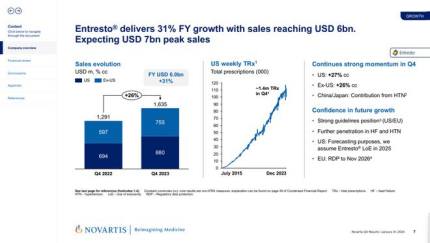
2024年上半年,诺华公司的诺欣妥继续保持强劲的增长势头,第一季度全球销售额超过了18亿美元,同比大增34%。然而,在国内外,仿制药竞争者针对诺欣妥的专利挑战不断,为了保护其知识产权和市场地位,诺华公司多次通过诉讼掀起专利保卫战,力图延长其专利保护期,保持市场竞争力。
仿制药浪潮汹涌
诺华能否捍卫市场壁垒?
在美国,诺欣妥/Entresto的专利保护网络覆盖了其配方的多个方面,确保了其专利保护期可至2036年。然而,即便拥有强大的专利保护,诺华同样面临着激烈的专利挑战。
此前,诺华提交了一份公民请愿书,请求FDA至少在2024年2月16日之前不要批准任何Entresto仿制药,这一时间表是基于2021年HFpEF适应症批准附带的额外三年独占期得出的。诺华认为,2024年之前批准的任何仿制药将违反FDA对仿制药的“相同标签”标准。当时,至少有18家制药商提交了寻求批准仿制Entresto产品申请,希望在2023年7月将他们的产品推向市场。
近期FDA驳回了诺华的请愿,这或将对Entresto原研药的市场独占权构成挑战,并可能加速仿制药的上市进程。
在对诺华公司的请愿书作出回应时,FDA明确表示,诺华请求在2024年2月16日之前不批准任何引用其心衰药物Entresto的申请是无效的。FDA指出,不论所谓的独占权覆盖范围如何,这些权利均已告终。此外,FDA也驳回了诺华关于Entresto专利保护的其他两个主要请求。FDA认为,仿制药的申请者可以通过适当调整其产品标签,来规避侵犯Entresto现有专利权的问题。这一裁决无疑为仿制药的进入打开了大门。
尽管FDA的裁决已经明确,但诺华公司并未放弃其立场。诺华在华盛顿特区的联邦法院对FDA提起诉讼,认为FDA批准MSN Laboratories的Entresto仿制药是违法的,FDA批准的仿制药标签“不恰当地更改了Entresto的批准适应症”,并且“省略了原研药标签中的一些关键安全信息”。同时指出,FDA批准的仿制药在活性成分上与Entresto并不完全一致。
事实上,这已不是诺华首次捍卫Entresto专利的行动。在2023年7月7日,诺华曾面临另一项挑战,当时Entresto的组合专利被特拉华州法院判定无效。对此,诺华表示将上诉至美国联邦巡回上诉法院(CAFC),力图逆转这一不利判决。

尽管诺华在法律上采取了积极的措施,但仿制药的入市浪潮似乎已不可阻挡。仿制药公司如MSN Laboratories已经获得了FDA的批准,正准备向市场推出Entresto仿制药版本。这一进展不仅对诺华构成了显著的市场竞争压力,而且可能对其未来的销售额和利润率产生深远的影响。
除了面临仿制药的竞争外,Entresto还被纳入了美国的《通胀削减法案》下的医疗保险药品价格谈判项目。这个法案意在通过政府与药品制造商的价格谈判来降低医疗保险覆盖药品的成本,这一价格谈判的最终结果预计将在9月1日公布。诺华公司表示,尽管面临价格谈判,但他们认为这一“价格设定计划”的影响将是“可控的”。
国内多个产品获批
市场争夺战一触即发?
在中国,Entresto同样面临专利挑战。
Entresto/诺欣妥在中国拥有三项已授权的专利保护,专利号分别为ZL200680001733.0、ZL201210191052.2和ZL201110029600.7,这些专利分别涵盖了固体复合物及其晶体形式(含2.5个结晶水)、固体复合物及其晶体(0-3个结晶水)和药物组合物。然而,这些专利都在国内面临了不同程度的挑战。
2017年,业内人士对涉及含有缬沙坦和NEP抑制剂的药物组合物的核心专利ZL201110029600.7发起了挑战。国家知识产权局专利复审委员会审查后,宣告该专利全部无效,主要理由是专利说明书公开不充分和发明不具备创造性。
此外,据国家知识产权局专利局公告,2019年之前,已有多家国内药企如石药集团欧意、齐鲁制药等对诺欣妥提出专利无效挑战,涉及沙库巴曲缬沙坦钠片的化合物和组合物专利。2021年7月2日,国家知识产权局发布三份公告,信立泰、正大天晴、石药欧意三家公司对诺欣妥的专利挑战获得部分成功,即组合物专利被认定无效,而晶型专利保持有效。
尽管面临挑战,诺华仍有晶型专利的有效保护,预计可以让诺欣妥在中国市场的独占期持续到2026年11月。
不过,2023年8月24日,南京方生和医药公司宣布其子公司南京一心和成功开发了一种新的晶型,其申报的沙库巴曲缬沙坦钠片(商品名“一心坦”)采用了含有3个结晶水的新晶型,规避了原研药Entresto的含有2.5个结晶水的晶型专利障碍。
对此,诺华公司立即官方发表声明:沙库巴曲缬沙坦钠的两项专利目前均处于有效状态。

无论一心坦能否提前上市,面对极具诱惑的巨大市场蛋糕,诸多国产药企加速布局,市场竞争的战线已经拉开。根据国家药监局药品查询数据,目前,我国已有13家企业有沙库巴曲缬沙坦钠产品获批,大战一触即发。

市场观点指出,尽管仿制药的竞争终将到来,但通过专利保护策略、市场深耕以及新的增长点拓展,Entresto还是可以为诺华带来持久可观的收益。
就像昔日的“药王”修美乐一样,尽管其关键专利在2016年底到期,但艾伯维却通过一系列精心策划的专利策略、谈判和诉讼手段,成功地延缓了阿达木单抗生物类似药的市场准入,从而维持了其在定价上的主导地位,使得修美乐的市场领导地位得以延续七年之久。
诺华在保护Entresto方面采取了类似的策略。自2019年10月以来,诺华在积极应对专利侵权的挑战。面对多家提交简化新药申请(ANDA)的公司,诺华不仅展开了诉讼,也通过与部分ANDA申请者达成和解协议。专利悬崖在前,Entresto/诺欣妥还能畅销多久?《医药经济报》将持续关注。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx