在围绕IL-4Rα靶点展开的免疫药物重磅炸弹产品竞争中,国内医药创新企业正在加速完成跟本土大药企的“交接”。
日前,大型综合性医药上市公司华东医药,与聚焦自免的Biotech荃信生物联合宣布,双方就荃信生物自主研发的重组人源化IL-4Rα单克隆抗体QX005N注射液签署合作开发及市场推广服务协议。

在大热靶点IL-4Rα上,目前国内仅有赛诺菲的度普利尤单抗获批上市。据赛诺菲年报,2023年度普利尤单抗全球收入增长33.49%,全球销售115.88亿美元,首次突破百亿美元,居2023年全球药物销售第五名。赛诺菲预测今年销售额将达到130亿欧元(140亿美元),已经成为当之无愧的“超级重磅”产品。
业界对于爆款产品的巨大市场空间不断投以期待。此前,国内康诺亚的IL-4Rα单抗CM301授权给了石药集团,康乃德的IL-4Rα单抗Rademikibart授权给了先声药业,此次又一国内大型制药公司加入“超级重磅”赛道竞逐,未来IL-4R市场战火将会异常激烈。
自免领域再度联手
争千亿呼吸新药市场
近几年,越来越多的企业加入到免疫疾病药物的研究与开发当中。作为可治疗多种自免疾病的靶点,IL-4R是目前开发最为火热的靶点之一。
QX005N是荃信生物开发的一款以人IL-4受体α亚基(IL-4Rα)为靶点的创新型人源化单克隆抗体,2024年1月被CDE纳入突破性治疗品种,用于治疗成人中重度结节性痒疹。其通过与IL-4Rα特异性结合,阻断IL-4Rα与IL-4以及IL-13的结合,同时抑制IL-4和IL-13介导的信号通路与生物学效应,从而对2型炎症过敏性疾病发挥治疗作用。
按照本次达成的合作,中美华东将深度参与QX005N注射液在授权区域(中国大陆、香港、澳门及台湾)内的后续临床开发并承担相关适应症50%的III期临床开发及后续注册费用;同时,中美华东将获得QX005N注射液在授权区域内的独家市场推广选择权。若选择权获行使,荃信生物将委托中美华东开展QX005N注射液的市场推广活动并向其支付推广服务费用;此外,中美华东也将获得该产品上市许可持有人转让的优先合作权。

目前,QX005N注射液已获得用于治疗成人中重度特应性皮炎、结节性痒疹、慢性鼻窦炎伴有鼻息肉等适应症的7项IND许可,于2024年1月被中国国家药品监督管理局(NMPA)药品审评中心纳入突破性治疗品种名单。QX005N注射液针对成人中重度特应性皮炎及结节性痒疹的两项3期临床试验均在入组中。
值得一提的是,本次合作是华东医药与荃信生物继共同开发QX001S(HDM3001)注射液后的再次联手。作为专注于自免产品研发的公司,荃信生物临床在研项目共9项,核心产品为QX001S、QX002N和QX005N,申报国内外专利70多项。
据了解,QX001S是荃信生物研发管线中进展最快的产品,是一种用于治疗银屑病(Ps)的IL-12/IL-23p40(白介素靶点)抑制剂,也是首个在中国提交生物制品许可申请(BLA)的国产乌司奴单抗(Stelara)生物类似药,并计划开发用于治疗溃疡性结肠炎及克罗恩病。
乌司奴单抗是由强生开发的靶向IL12/23 p40亚基的单抗,用于治疗银屑病、银屑病关节炎、溃疡性结肠炎等。2022年,乌司奴单抗全球销售突破百亿大关,达102亿美金。
QX001S预计将在今年第四季度推向市场,为确保QX001S成功商业化,荃信生物与华东医药就QX001S在中国的联合开发及独家商业化订立战略合作协议,荃信生物获得的首付款及里程碑付款合计为5000万元,且未来将通过分成的形式取得QX001S国内税前利润的一半。华东医药的商业化能力预期将为荃信生物提供销售上的有力支持。
业内观点认为,自免疾病机制复杂,新靶点药物的药效和毒副作用评估难度大、研发存在壁垒,治疗方法与商业化模式和肿瘤有巨大差异。因此,国内入局自免产品研发的企业中,深耕者仍是少数。在国内,自免药物市场仍充满不确定性。
石药、先声领跑
免疫领域“超级重磅”将洗牌?
IL-4Rα药物因独特的药理特性和临床应用前景,市场潜力巨大。弗若斯特沙利文报告显示:全球IL-4Rα靶向疗法的市场规模预期将于2030年达到287亿美元,我国IL-4Rα靶向疗法市场规模预期将于2030年达到282亿元人民币。
每一次细分领域的局部市场洗牌,也考验着本土医药企业在技术、团队、执行力、创新力等方面的综合实力,从而让一批极具潜力的创新公司实现跨越式发展,最终脱颖而出。
除了赛诺菲的度普利尤单抗(中文商品名:达必妥),目前国内药企研发进度居前的是石药与康诺亚的司普奇拜单抗(国内已经申报上市)、先声药业与康乃德生物医药的rademikibart(处于Ⅲ期临床)。
2021年3月,康诺亚与石药集团签订协议,授权石药集团司普奇拜单抗在中重度哮喘和慢性阻塞性肺病(COPD)等呼吸系统疾病的独家开发及商业化权利。根据协议,石药集团向康诺亚支付了7000万元的首付款和1亿元的开发里程碑付款。
2023年11月21日,先声药业和香港康乃德生物医药宣布双方就创新药IL-4Rα单抗Rademikibart订立独家许可与合作协议。根据协议,康乃德将获得1.5亿人民币预付款,在实现特定的开发和商业里程碑后将获得高达8.75亿人民币(约合1.2亿美元)的付款,此外还将获得高达净销售额两位数百分比的特许权使用费。先声药业集团将获得在大中华地区开发、生产和商业化该产品所有适应症的独家权利。
值得关注的是,康方生物、三生国健、智翔金泰和恒瑞医药等均在加紧国产IL-4Rα单抗研发脚步。
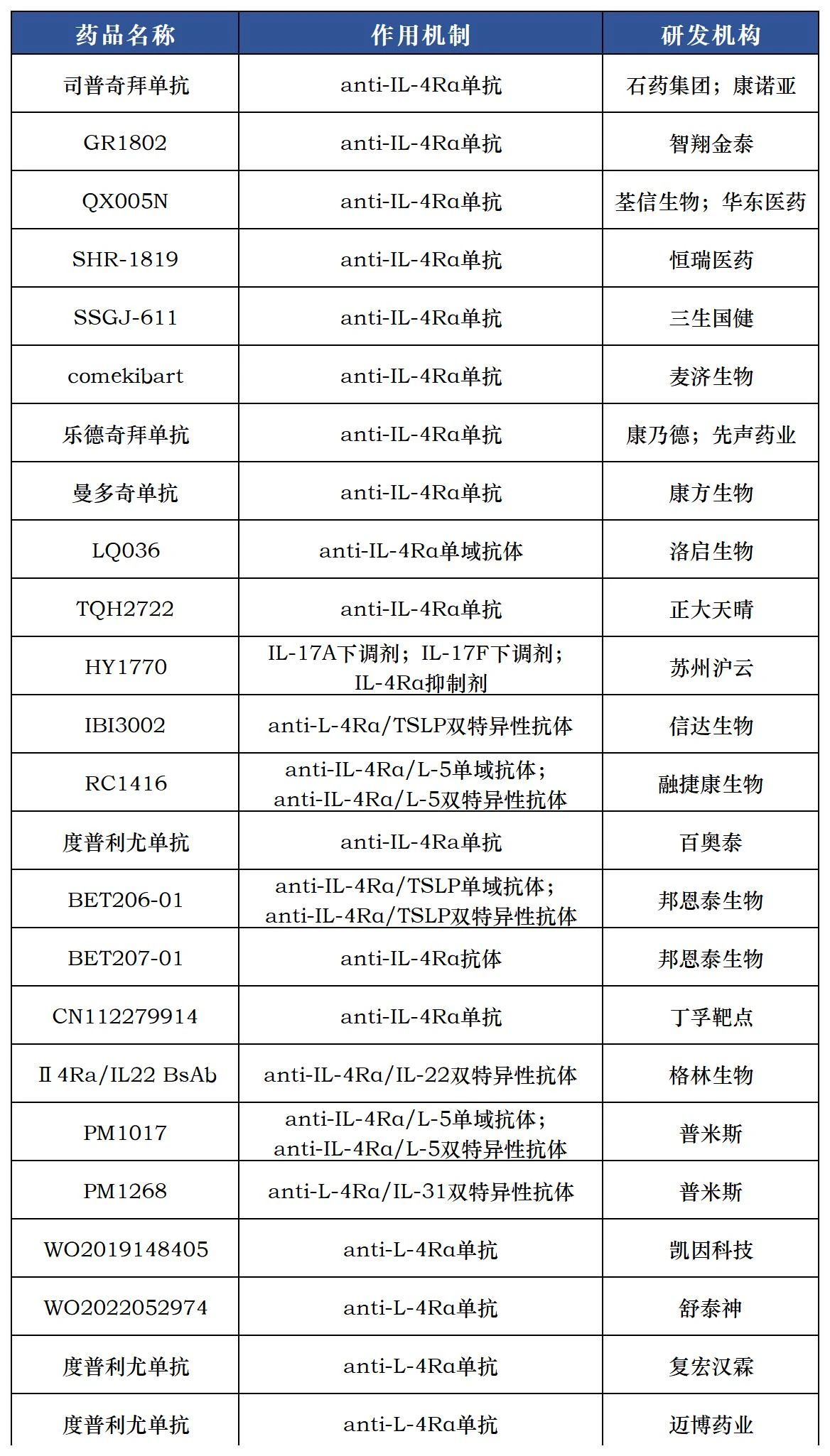
行业观点分析指出,国产IL-4R未来上市,将不仅丰富中国自身免疫疾病治疗市场的药物种类,还可能因其较为亲民的价格,提高药物的可及性和患者的用药依从性,并且进一步促进本土生物医药技术的发展,增强国内企业在全球医药市场的竞争力。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx