近日,CDE官网公示,拜耳(Bayer)申报的BAY 2927088拟纳入突破性治疗品种,适用于治疗携带HER2(ERBB2)激活突变且既往接受过一种全身性治疗的不可切除或转移性非小细胞肺癌(NSCLC)成人患者。
根据拜耳公开资料,BAY 2927088是一种口服、可逆、非共价的酪氨酸激酶抑制剂(TKI),对HER2 20号外显子插入和HER2点突变,以及表皮生长因子受体(EGFR)突变有高效力和选择性。针对本次被CDE拟纳入突破性治疗品种的适应症,BAY 2927088已经于今年2月获美国FDA授予突破性疗法认定,其临床研究数据也入选了今年美国临床肿瘤学会(ASCO)年会最新突破摘要(LBA)。
在今年的ASCO大会上,研究人员还以口头报告(LBA摘要)的形式公布了BAY 2927088的1/2期研究扩展队列SOHO-01的结果。该试验主要评估了BAY 2927088对HER2突变型NSCLC患者的安全性和抗肿瘤活性。
有效性数据显示,在33名可评估疗效的患者中:23名患者出现反应,客观反应率(ORR)为70%;5名患者(15%)病情稳定,疾病控制率为82%;中位反应时间为5.7周,反应迅速且持久(中位反应持续时间未达到);中位无进展生存期为8.1个月。
HER2突变与肺癌
在罕见靶点中,HER2基因突变在肺癌的发生率为2%-4%,在非小细胞肺癌中占1%~2%左右,是一种较为少见的肿瘤驱动基因,虽是罕见,但是基于我国庞大的肺癌患者基数,这种罕见却并不"少见"。而且,其在亚洲患者比例相对较高,而且从HER2突变肺癌患者的临床特征来看,主要见于非吸烟者、年轻女性和腺癌患者,且容易出现脑转移,预后较差,更值得引起关注。
HER(human epidermal receptor,人表皮生长因子受体)家族属于四个密切相关的 I 型受体酪氨酸激酶(RTK)家族胞膜受体之一,与多种肿瘤的发生和发展密切相关。HER 家族主要有四个结构类似的受体分子,包括 ErbB-1(又称 EGFR,HER1)、ErbB2(也称为 Neu,HER2)、ErbB-3(HER3)和 ErbB-4(HER4)四个成员。HER2 与 EGFR 同属于人类表皮生长因子受体家族,主要参与 PI3K/AKT 和 MEK/ERK 通路磷酸化和活化。
非小细胞肺癌(NSCLC)中HER2变异主要有两种形式:一是HER2基因扩增;二是HER2基因激活突变。HER2基因突变的患者,占所有肺腺癌患者的1.7%,所有EGFR、KRAS、ALK突变阴性患者的6%,这其中96%的患者都表现为20号外显子的插入突变(最常见的形式是HER2基因第20号外显子第775位插入了YVMA四个氨基酸)。
肺癌抗HER2 治疗: 小分子靶向药前景可期
ADC等新型药物的问世,看似给HER2突变NSCLC患者带来希望,但几乎所有患者在治疗时均会出现治疗相关不良反应(TRAE)。此外,非选择性泛HER抑制剂肿瘤应答率低或无应答,患者OS和PFS未得到改善,且不良反应突出。因此,高效选择,精准靶向新型药物的研发迫在眉睫。
前文提到过HER2与EGFR同属ERBB家族有相近的关系,这也使得HER2激活突变,尤其是HER2 20插入的治疗与EGFR 20插入的治疗有些许类似,二者可使用的药物相似度很高。
针对EGFR20插入突变有三款药物上市。而HER2 ex20ins突变肺癌,目前没有任何靶向药物获批上市,标准治疗仍然是含铂双药化疗。
第一款获批药物是强生的埃万妥单抗,为静脉输注给药,并没有在国内上市。
第二款是武田制药的莫博替尼(Exkivity),是获批的第一个口服药物,2021年9月其二线适应症获得FDA加速批准,2023年1月11日在中国获批。在美国的限制性条件是一线治疗EXCLAIM-2Ⅲ期临床试验作为确证性试验,如果成功,会将"加速批准"转为"完全批准"。然而遗憾的是,Ⅲ期EXCLAIM-2试验结果失败,Exkivity折戟沉沙。武田曾经预测这款药物的最高销售额为3亿~6亿美元,面对这个结果,武田没有选择撤回二线适应症,而是直接将产品撤市。
第三款药物是来自迪哲药业的舒沃替尼,2023年8月刚刚在国内获批。
而HER2 ex20ins突变肺癌,目前没有任何靶向药物获批上市,标准治疗仍然是含铂双药化疗。如今已有多款针对肺癌EGFR 20ins TKI正在同步开展HER2 20ins的临床研究,前期临床研究中均展现出出色数据。此外,恒瑞研发的泛HER2 TKI 吡咯替尼也在HER2突变的NSCLC显示出临床获益。
据不完全统计,目前在研针对HER2 20ins在研的药物不足10种,其中多数是针对EGFR/HER2 20ins设计。
值得格外关注的是,同样入选了今年ASCO年会摘要的另一款明星HER2 TKI Zongertinib。Zongertinib是一种共价结合、口服有效的选择性HER2小分子抑制剂,与野生型和突变型HER2受体(包括20号外显子突变)的酪氨酸激酶结构域(TKD)共价结合,同时保留EGFR野生型信号,在保证疗效的基础上,兼具良好的耐受性及安全性。
Beamion LUNG-1是一项正在进行中的Ia/Ib期临床研究,探索Zongertinib单药治疗HER2变异晚期实体瘤患者最大耐受剂量(MTD)、剂量限制性毒性(DLT)及初步疗效。
ASCO 2024数据显示,截至2024年1月29日,共83例患者接受了Zongertinib治疗。在74例可评估患者中,ORR和DCR分别达到35%和85%。在41例可评估的NSCLC患者中,ORR达到44%,DCR达到93%。在41例可评估HER2突变患者中,ORR/DCR分别达到56/93%, 其中34例HER2 TKD突变患者的ORR/DCR分别为62/94%,而16例A775_G776insYVMA突变患者的ORR/DCR分别为69/94%。总体中位缓解持续时间(mDoR)为12.7个月。NSCLC患者mDoR达15.8个月。数据截止时,仍有45.8%的患者继续治疗。总体而言,Zongertinib在HER2突变阳性的晚期NSCLC患者中表现出极为卓越的疗效数据,且耐受性良好。
目前其III期研究Beamion LUNG-2进一步对Zongertinib一线治疗局部晚期/转移性HER2突变阳性NSCLC患者的疗效和安全性进行探索。
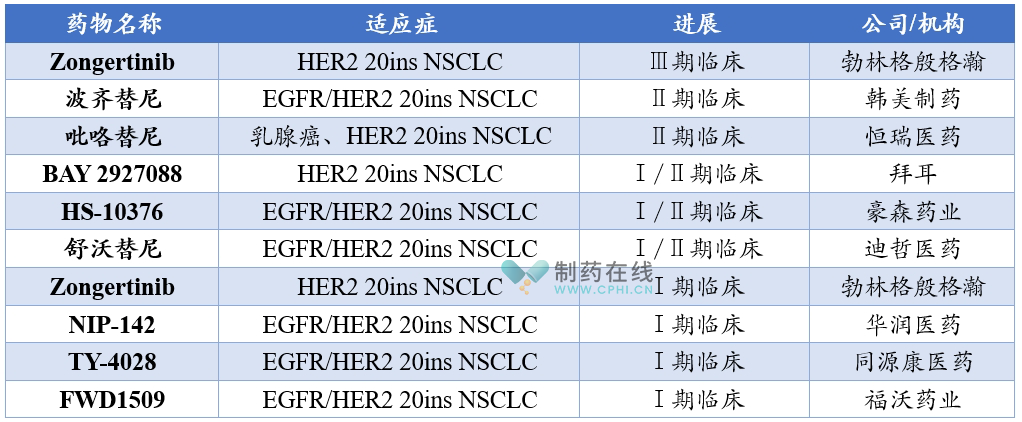
全球部分在研 HER2 20ins TKI
结语
HER2激活突变占到非小细胞肺癌患者的2-4%,目前还缺乏FDA完全批准的治疗方案。现在已有多款新型TKI在HER2激活突变突变患者中展现出极高的客观缓解率(高于HER2 ADC),期待后续完善大型Ⅲ期临床进一步验证,未来相信必将改写肺癌抗HER2临床治疗格局,更给肺癌少见靶点患者带来新的希望。
参考来源:
1. Cornelissen R, et al., on behalf of the ZENITH20-4 Investigators, Poziotinib in Treatment-Na?ve Non-Small-Cell Lung Cancer Harboring HER2 Exon 20 Mutations: ZENITH20-4, A Multicenter, Multicohort, Open-label Phase 2 Trial (Cohort 4), Journal of Thoracic Oncology (2023).
2. John Heymach,et al.2024 ASCO Rapid Oral Abstract Session S406.Abstract 8514
3. Melissa Johnson,et al.2024 ASCO Poster Bd #: 515a.Abstract TPS8654
4. Uy NF, et al. Cancers (Basel). 2022 Aug 27;14(17):4155.
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx