为期四天的第42届摩根大通医疗健康年会(JPM)在美国旧金山如期举行,每年JPM前后,大型跨国制药企业畅谈新战略,力求在新年伊始把握并购和交易的先机。
近日,默沙东首席执行官Rob Davis在一次行业交流会议上表示,默沙东对不仅能改善体重,而且还能在心脏病和脂肪肝等其他领域带来益处的GLP-1联合用药方案感兴趣,或将寻求交易。

医保很难为减肥买单,Davis认为,GLP-1联合用药方案可能会使药物的报销更容易。他说:“体重管理是一件很难报销的事情。但如果这个疗法能展示出心血管疾病、糖尿病的治疗效果……我们认为这是一个有机会的领域。”
去年9月,摩根大通更新了对GLP-1受体激动剂类产品的市场预测,分析师Richard Vosser估计,到2032年,全球减重市场将达到710亿美元,其中诺和诺德和礼来各占整个销售额的45%。该预测是摩根大通此前估计的市场规模两倍多。
默沙东显然不能坐视诺和诺德和礼来两家独大,瓜分掉90%的市场份额。目前,默沙东手上的GLP-1药物efinopegdutide正在肥胖、糖尿病和非酒精性脂肪性肝炎(NASH)中进行研究,如能展示出减肥之外的好处,并以此获得医保报销资格,默沙东寄希望能够在GLP-1的市场赛道中实现赶超。
默沙东的GLP-1药物efinopegdutide(MK-6024)是韩美公司开发的一种合成的、经修饰的胃泌酸调节素(OXM)肽,是一种作用于GLP-1R和GCGR的双重激动剂。
2020年8月,默沙东与韩美签订了独家许可协议。根据协议,默沙东将获得efinopegdutide在美国和全球范围内开发、制造和商业化的独家许可。韩美获得1000万美元的预付款,并有资格获得与efinopegdutide开发、监管审批及商业化有关的最高8.6亿美元的里程碑付款,以及基于产品销售额的两位数版税。
与其他GLP-1赛道企业不同的是,默沙东拿下efinopegdutide后并没有加入对2型糖尿病和肥胖症的追逐,而是另辟蹊径,核心攻关非酒精性脂肪性肝炎(NASH)。
值得一提的是,此前韩美曾以1.05亿美元的预付款将efinopegdutide授权给强生制药,不过在2019年,尽管针对肥胖症的II期临床试验数据达到了减重指标,但肥胖合并糖尿病患者的血糖控制未能让强生满意,强生将产权退还给韩美。
2023年6月12日,默沙东宣布efinopegdutide获得FDA的快速通道认证,用于治疗NASH。
NASH是非酒精性脂肪性肝病(NAFLD)的严重类型,被定义为5%以上的肝脏脂肪变性,合并炎症、肝细胞损伤,伴有或者不伴有纤维化。
肥胖和2型糖尿病是NAFLD/NASH发生的主要因素。随着研究者对GLP-1靶点研究的深入,发现GLP-1与肝脏细胞受体结合后能降低肝脏脂肪变性、肝细胞损伤和葡萄糖输出,在NASH中能减低肝细胞炎性反应和纤维化。
2023年6月23日,默沙东在欧洲肝脏研究协会(EASL)年会上口头报告了efinopegdutide治疗NAFLD成人患者的2a期研究数据。该2a期试验选取了司美格鲁肽(1.0mg剂量)作为对照组。接受efinepegdutide治疗的患者在第24周平均肝脏脂肪含量相对降低比例显著高于司美格鲁肽对照组(-72.7% vs -42.3%)。在减轻体重方面,24周后efinopegdutide组体重平均减轻8.5%,司美格鲁肽对照组为7.1%(p=0.085)。
不过,有分析师指出,试验中司美格鲁肽的剂量为1.34 mg/mL,而efinepegdutide的剂量为20mg/mL。因此,司美格鲁肽如果提高剂量有望实现更优的效果。
稍早时候,2023年6月7日,默沙东在临床试验登记网站Clinicaltrials.gov更新了efinopegdutide在NASH适应症上的2b期临床试验设计方案。根据方案,2b期将入组300人。默沙东为efinopegdutide选择了两个对照组,一组是常规的安慰剂,另一组则是司美格鲁肽。
业内人士指出,默沙东在糖尿病和减肥领域相对落后,即使在NASH领域,司美格鲁肽也是目前进展最快的药物,有望在NASH适应症全球率先撞线获批,但默沙东显然对自家的双靶点药物信心更足,能够在头对头中击败司美格鲁肽。
GLP-1正在慢病领域不断拓展,司美格鲁肽凭借心血管结局获益先下一城。
2023年11月11日,诺和诺德在美国心脏协会(AHA)科学会议上公布了司美格鲁肽的2.4mg剂量心血管获益的三期临床试验SELECT最新数据,同时这些数据也在新英格兰医学期刊(NEJM)上发表。

SELECT试验共有17604名受试者入组,患有心血管疾病与超重或肥胖症,但不患有糖尿病。其中8803人接受了司美格鲁肽(2.4mg)治疗,8801人接受安慰剂治疗。平均用药持续时间为34.2±13.7个月,平均随访时间为39.8±9.4个月。
结果显示,与安慰剂相比,2.4mg的司美格鲁肽能在长达五年的时间里将主要不良心血管事件(MACE)风险显著降低20%。
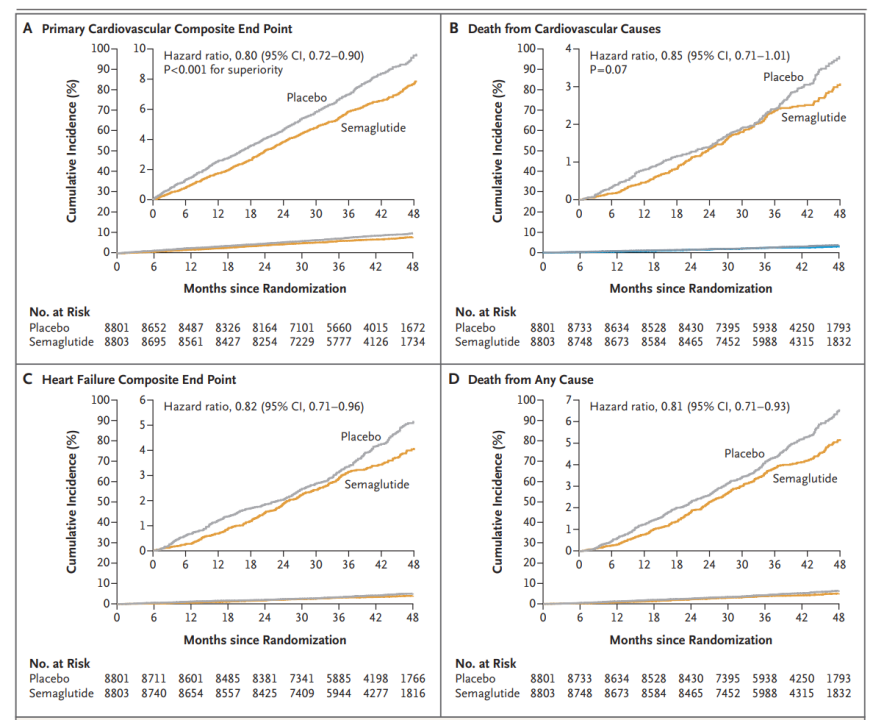
而且,在MACE风险降低方面,司美格鲁肽获益在治疗开始后不久即得以显现,这提示司美格鲁肽的心血管获益很可能并不单纯来自患者体重减轻。
据了解,诺和诺德已在美国和欧盟申请更新Wegovy(即减重版司美格鲁肽)的标签,拓展“降低患有肥胖症和已确诊心血管疾病的成年患者的MACE风险”的适应症。目前,FDA已授予Wegovy优先评审资格。
在双靶点赛道,礼来GIPR/GLP-1R双重激动剂Tirzepatide(替尔泊肽)正在不断刷新着市场对减肥药物的认知和预期。
2023年10月,礼来SURMOUNT-3 临床研究的详细结果在《Nature Medicine》和2023肥胖周上同步发表。该研究评估了替尔泊肽(Tirzepatide)针对肥胖或伴有至少一种合并症的超重非2型糖尿病成人患者的有效性与安全性。在72周的双盲研究期间,替尔泊肽达到了两个共同主要终点,证明其优效于安慰剂。

目前,替尔泊肽正在同步进行肥胖相关合并症的多项Ⅲ期研究,包括SURMOUNT-MMO研究(减少肥胖合并症及死亡风险)、SURMOUNT-OSA研究(阻塞性睡眠呼吸暂停)、SURMOUNT-NASH研究(非酒精性脂肪性肝炎)、TREASURE-CKD研究(慢性肾病)、SUMMIT研究(射血分数保留的心衰)、SURPASS-CVOT研究(心血管风险)等。
同时,礼来也启动了头对头比较替尔泊肽与司美格鲁肽减肥作用的Ⅲ期SURMOUNT-5研究,预计2024年末完成。
值得一提的是,为了加强终端覆盖,礼来近期全面发力线上宣传和患者服务,为了满足用药需求,1月4日,礼来推出了端到端的数字化医疗服务平台LillyDirect,将为美国肥胖症、偏头痛和糖尿病患者提供全新的数字医疗服务体验,包括:与独立医疗服务供应商的联系、量身定制的治疗方案以及通过第三方药房配药服务,将礼来特定的药品直接送货上门。
除了默沙东以外,同样在错失GLP-1潮起风口后考虑组合疗法的还有阿斯利康。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx