全球畅销药物背后的专利权争夺战愈演愈烈,战火已经开始从PD-(L)1、CAR-T向的ADC赛道蔓延。
日前,第一三共公布了其2023年财年前六个月(2023年4月至9月)的财务业绩:总营收7263.44亿日元(按2023财年汇率1美元=130日元计算,约为55.87亿美元),同比增长19.5%。其中,HER2 ADC德曲妥珠单抗(Enhertu,DS-8201)总收入1830亿日元(14.08亿美元),同比增长81.2%,包括1734亿日元(13.34亿美元)全球销售额以及91.5亿日元(0.70亿美元)的预付款和里程碑付款。

不过,这款重磅ADC的全球销售额或将不能悉数装进第一三共的“口袋”。
第一三共近期发布新闻稿称,美国德克萨斯州东部地区地方法院对其与Seagen之间的专利诉讼作出了修改后的最终判决:除了此前陪审团裁决后法院裁定的4180万美元赔偿金以外,还要求第一三共向Seagen支付从2022年4月1至2024年11月4日(美国专利10,808,039到期时间)销售德曲妥珠单抗的8%分成,作为专利许可费。

ADC药物是目前抗肿瘤药物领域最热门的研发方向之一,第一三共开发的DS-8201塑造起了新一代的药物标杆,将ADC的临床效果推向另一个量级,让这一赛道的想象空间更加巨大。但在市场火热背后,ADC药物因更复杂的结构设计,其专利风险如影随形。专利的布局和设防对创新药物的销售市场起着决定性作用,第一三共和Seagen之间多年的ADC专利诉讼只是其中一道缩影,也为国内相关玩家的布局和出海提了个醒。
从七年合作走向对簿公堂
成立于1998年的Seagen可谓是ADC领域的“元老级”公司之一,作为ADC技术的开拓者,其先后与基因泰克、拜耳等生物技术和制药企业达成开发合作,这也让彼时大约三分之一经FDA批准和上市的ADC产品都使用了Seagen的技术。而Seagen与第一三共之间的这起专利纠纷案,同样要追溯至15年前的一次授权合作。
2008年7月,Seagen宣布与第一三共签订全球独家合作协议,共同开发针对多种类型实体肿瘤的单一抗原ADC产品。根据合作条款,Seagen将获得400万美元的预付款,以及与进展相关的里程碑付款,以及由此产生的ADC产品全球净销售额的中位数版税。第一三共将负责所有ADC产品的研究、产品开发、制造和商业化。Seagen将获得材料供应和年度维护费,以及为第一三共开发ADC产品提供帮助的研究支持付款。

正是在这次合作中,Seagen授予了第一三共在ADC产品开发中使用其细胞毒素和接头技术的许可。通过由第一三共提供抗体化合物,Seagen提供连接子技术,双方携手展开了在ADC领域的多年探索。另外,公开资料显示,根据协议,双方约定在共同研发期间对技术上的改进,Seagen有权获得这部分专利。
然而,新药开发的路上总是充满着未知,因ADC产品开发项目没有太多实质性进展,双方在2015年6月底便终止了这项合作,不过各自都在这条赛道上继续探索。值得一提的是,随后在2015年9月,第一三共就启动了DS-8201的首项I期临床试验DS8201-A-J101研究(NCT02564900),对该药的安全性和药代动力学等基本性质进行确定,同时这奠定了DS-8201在HER2表达或突变肿瘤适应症的开发方向。
尽管Seagen随后也注意到了在临床开发上一路高歌猛进的DS-8201,其间也试图开发自己的基于拓扑异构酶抑制剂的ADC技术平台,但最后并未成功。直到第一三共的DS-8201受到全球制药巨擘阿斯利康的关注后,Seagen才在合适的时机发起了反击。
2019年3月,阿斯利康与第一三共宣布就DS-8201签订全球开发和商业化合作协议,双方共同负责DS-8201在全球(日本除外)的开发和商业化,第一三共保留在日本的市场专有权并全权负责生产和供应。为此,阿斯利康向第一三共支付13.5亿美元首付款,以及后续的研发注册和商业里程金额,交易金额总计69亿美元。本次合作创下ADC领域的一大交易纪录,更是直接点燃了ADC领域的投资热情。
此次交易后,Seagen先是利用美国专利法特色的接序案(CA制度)提交了一份专利(US20190338045A1)修改申请,为后续发起的专利诉讼做好准备;另外一方面则强势要求第一三共转让双方曾经合作期间由第一三共研发的专利。断然拒绝且协商不成的第一三共在2019年11月向Seagen提起诉讼,而Seagen在同月则是直接进一步提起仲裁请求,两大巨头的专利大战自此展开。


在这纸诉状中,Seagen认为,第一三共在DS-8201等这些候选药物中使用的连接子和其他ADC技术是对其开创性ADC技术的改进,根据两家公司2008年合作协议的条款,该技术的所有权已转让给Seagen。第一三共则认为任何此类声明都是没有根据的,其ADC技术专利是自己独家的知识产权。为此,双方展开了旷日持久的拉锯战。
2022年4月,美国德克萨斯州东区地方法院的陪审团裁定,第一三共在美国销售其DS-8201侵犯了Seagen专利(美国专利10,808,039)而被判赔偿4182万美元。此外,Seagen将要求第一三共在专利有效期内为DS-8201在美国的未来销售支付额外的特许权使用费。但第一三共不满判决结果提出上诉,2022年7月,美国德克萨斯州法院对第一三共和Seagen的专利法律纠纷重审作出判决,第一三共依旧被判败诉,但紧接着其再次提出上诉。
不过,第一三共这一次却实现了剧情反转。在2022年8月举行的三审终审判决上,仲裁员以违约诉讼时效已过和与Seagen在双方合作合同的解释上存在分歧为由,做出了有利于第一三共的裁决。这判决让第一三共不仅不用赔偿4182万美元,还被允许保留了其ADC药物的相关专利权,也不需要向Seagen支付专利使用费。
令第一三共没想到的是,这份终审判决在一年之后却再次发生反转。根据新闻稿,地方法院在驳回了第一三共提出的作为法律问题的判决请求或重新审判,并解决了请求澄清先前命令的动议后,作出了这次修改后的最终判决。此外,这次地方法院还驳回了Seagen要求支付律师费的要求。但这还不是这起专利纠纷案的终章,第一三共明确表示打算对修改后的最终判决提出上诉。
创新药的竞争本质是专利权的竞争。可以看到,Seagen为自家ADC Linker技术逐步建立的专利丛林,是这起纠纷能够取胜的关键。有业内人士指出,涉诉专利的美国临时申请最早是在2003年提交的,其正式申请是于2004年提交,即US7,498,298。针对该美国申请,Seagen提交了4个分案申请,其后续运用分案申请和延续申请策略,一直保持至少一件处于未决状态的申请,等待竞争对手的产品开发进度,根据对手产品的开发进度来决定如何修改权利要求,以便在权利要求中囊括竞争对手的产品,从而达到阻挡对手的效果。
ADC领域竞争进入下半程
现阶段,全球制药行业的研发重心正在向开发用于肿瘤治疗的ADC药物转变,这类药物特殊的结构设计使得其拥有多功能性和改变未来肿瘤治疗的潜力。值得注意的是,HER2阳性乳腺癌仍是目前ADC领域的主要关注点,但这些药物对不同种类的癌症有效这一事实表明,其将有能力作为其他具有高度未满足需求的癌症类型的可行治疗选择。
Seagen和第一三共毋庸置疑是这个新兴领域中最重要的两位参与者,前者已推出包括Adcetris、Padcev、Tivdak在内的三款ADC产品上市,而后者则是推出了具有碾压优势的DS-8201。GlobalData预测,ADC药物在肿瘤领域的全球市场规模有望在2029年超过360亿美元。其中,第一三共的销售额将突破100亿美元,远超同领域的其他玩家。
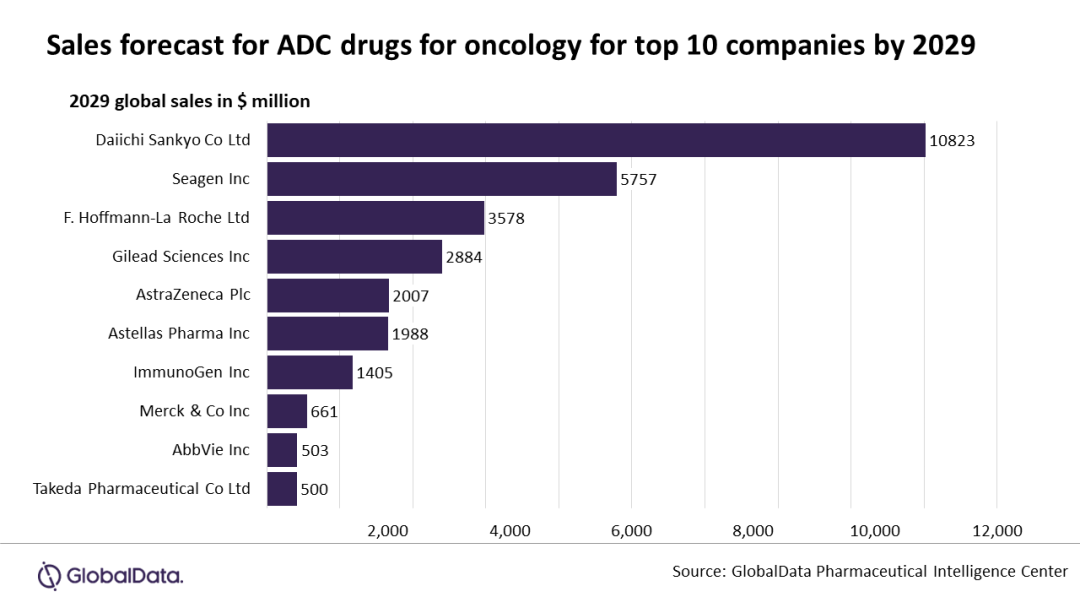
第一三共在ADC领域的实力和优势毋庸置疑,DS-8201作为其当家花旦,在朝着成为贯穿乳腺癌治疗全程的临床用药这一目标迅速迈进的同时,也在继续打破传统HER2靶向药物的局限,基于生物标志物不同表达水平,将治疗范围拓展至胃癌、非小细胞肺癌、胆道癌、膀胱癌等更广领域的探索,持续释放着在泛肿瘤治疗领域的巨大潜能。
除了DS-8201,第一三共基于其独特的DXd-ADC技术平台,仍在持续开发具有竞争力ADC产品。在研发管线中,第一三共还有其他6款在研ADC产品,其中Dato-DXd(datopotamab deruxtecan)和HER3-DXd(patritumab deruxtecan)均进入III期临床阶段。
今年10月,第一三共已将旗下3款ADC候选产品HER3-DXd、I-DXd(ifinatamab deruxtecan)和R-DXd(raludotatug deruxtecan)授权给默沙东。默沙东将支付45亿美元预付款、10亿美元的研发费用相关可退还预付款,以及最高165亿美元的商业里程碑金额,协议总金额高达220亿美元,再次刷新由第一三共和阿斯利康在2019年创下的ADC领域交易记录。在默沙东的加持下,第一三共在2025财年肿瘤业务销售收入将突破9000亿日元(69.2亿美元)的梦想正在加速实现。
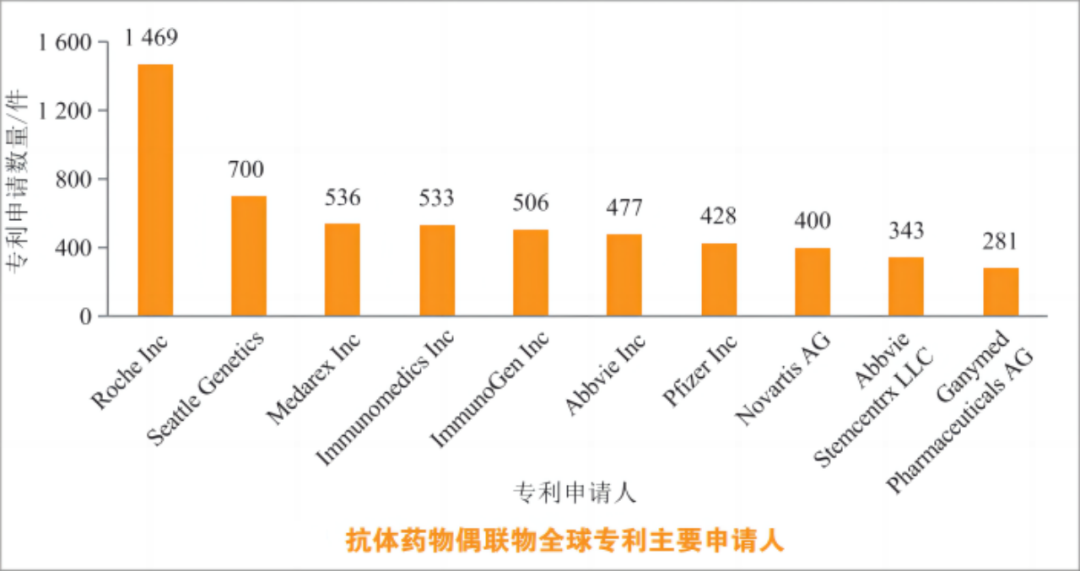
(来源:《药学进展》)
Seagen作为ADC领域的技术先驱,在ADC药物的专利申请数量方面仅次于罗氏,并且这些专利覆盖全面,包括抗体、连接子、小分子毒素及产品的医学用途等。在充实的技术积累下,Seagen已经推动三款ADC产品上市:在2011年,其和武田制药联合开发的靶向CD30的Adcetris成功获批上市,成为全球第二款获批的ADC药物;在2019年,其与安斯泰来合作开发的靶向Nectin-4的Padcev获批上市;在2021年,其开发的靶向组织因子(TF)的Tivdak获批上市,用于治疗复发或转移性宫颈癌患者,也是治疗这一患者群体的首款获批ADC。
根据最新发布的2023年第三季度财报,Seagen在今年前九个月的总营收为17.72亿美元,净产品销售总额为15.83亿美元,同比增长27%。其中,Adcetris贡献了7.51亿美元,同比增长25%;Padcev贡献了4.79亿美元,同比增长46%,这得益于今年4月其与帕博利珠单抗联合用于治疗不适合接受含顺铂化疗的晚期尿路上皮癌患者的一线治疗适应症的获批,仅第三季度就实现了2亿美元的营收贡献,同比增长89%;而Tivdak的市场潜力也还在释放,贡献了0.64亿美元,同比增长42%。
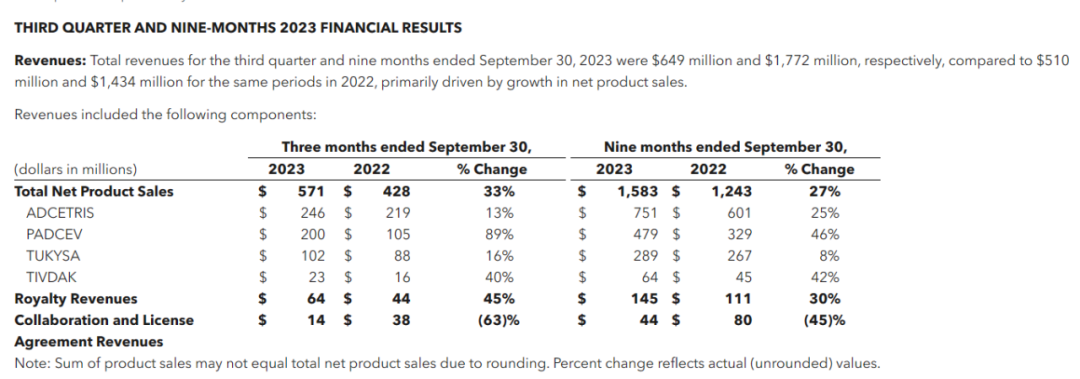
Seagen的研发管线除上述三款ADC和一款靶向HER2的口服小分子酪氨酸激酶抑制剂Tukysa(Tucatinib,妥卡替尼)已经上市的产品外,还有一款从荣昌生物引进的、靶向HER2的维迪西妥单抗(Disitamab Vedotin)正处于临床Ⅲ期。2021年8月,Seagen以2亿美元首付款以及最高24亿美元里程碑付款,和荣昌生物达成合作,共同开发及商业化维迪西妥单抗。今年第三季度,Seagen启动了一项Ⅲ期临床试验,评估维迪西妥单抗联合帕博利珠单抗与化疗在先前未治疗的局部晚期或转移性her2阳性尿路上皮癌患者中的疗效。
即使是ADC领域最资深的“元老级”企业,Seagen同样也害怕被第一三共这样的挑战者颠覆。因此,未雨绸缪的Seagen开始押注下一个ADC药物。今年9月,Seagen与PROTAC领域的领军企业Nurix达成了总价高达34.6亿美元的合作,希望研发出具有新作用机制的降解抗体偶物(DAC)。更令业界期待的是,辉瑞以430亿美元收购Seagen的提议近期已获得欧盟反垄断机构的无条件批准,Seagen预计该交易将于2023年底或2024年初完成。通过双方的技术合作和资源协同,Seagen有望开辟新的发展篇章。
Seagen和第一三共两大巨头的专利纠纷预示着ADC领域的市场竞争已经步入新的阶段,根据Global Data数据,仅在过去三年,制药行业就围绕着ADC药物申请和授予了63.3万项专利。值得注意的是,过去跨国药企全球专利布局常常会遗忘中国市场,这让本土药企躲过了百时美施贵宝掀起的海外PD-(L)1专利大战。但新一代ADC的专利布局不同,以第一三共为代表的跨国药企等在国内进行了缜密的布局。
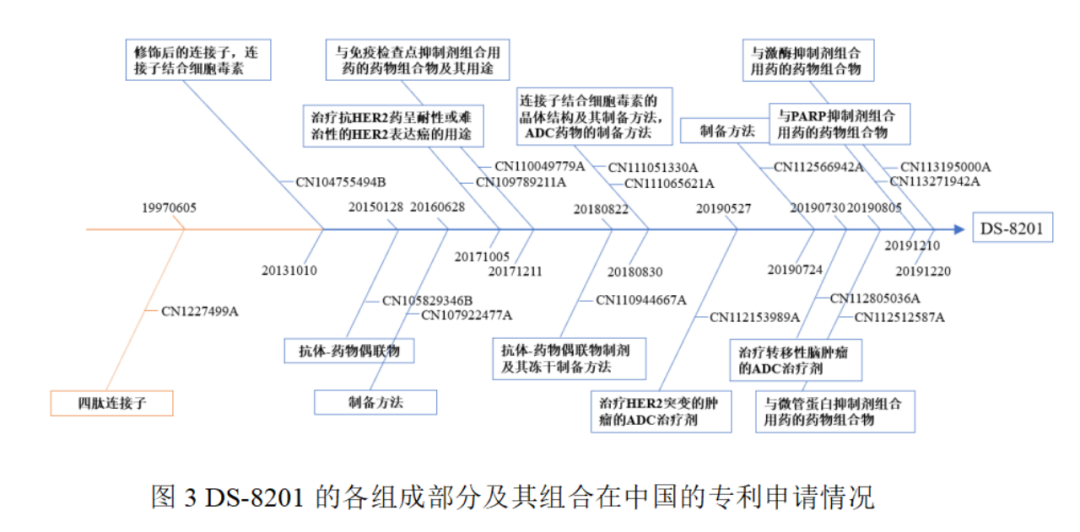
(来源: 汉坤律师事务所)
以DS-8201为例,从连接子、修饰后的连接子、连接子结合细胞毒素等各组成部分,以及与免疫检查点抑制剂、激酶抑制剂、PARP抑制剂等组合疗法,第一三共均在国内作了与美国相似且详细的专利申请和布局。例如中国授权专利CN104755494B保护了一种抗体偶联物,限定了小分子药物的具体结构和Linker的结构通式,并未对抗体做任何限定,保护范围非常宽泛。在不考虑药品专利期限补偿的情况下,该专利将于2033年10月到期。
基于先发优势,第一三共更可能依据药物结构及用途申请较广范围的权利保护要求,以限制后来者的研发追赶。与此同时,随着DS-8201在国内适应症的加速拓展,第一三共对于国内ADC药物的专利审视势必会更加细致,其与Seagen之间的专利纠纷未必不会同本土企业在国内上演。此外,本土创新药企出海之路愈加顺畅,但获得药品监管机构的批准上市只是敲门砖,上市以后还将面临海外专利的挑战。面对这些专利风险,本土药企应当做好准备。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx