10月27日,NMPA发布最新一批药品批准证明文件送达信息(详见今日次条),其中,江苏万邦生化的4类仿制化药甲磺酸奥希替尼片获批上市,斩获首仿+首家过评。


截图来源:NMPA官网
甲磺酸奥希替尼片(以下简称奥希替尼)原研来自阿斯利康,是其当家花旦,最早于2015年11月13日在美国获批上市(商品名:Tagrisso),是全球首个获批上市的、唯一获批一线治疗适应证的第三代 EGFR-TKI 靶向治疗药物。2022年,奥希替尼全球销售额达54.5亿美元,居阿斯利康产品销售额榜首,同时也是全球第六大抗肿瘤药物。2023年上半年,奥希替尼销售额达29.2亿美元,全年有望突破60亿美元。
而在国内,奥希替尼于2017年3月获批上市;2018年10月,奥希替尼通过“抗癌药医保准入专项谈判”进入国家医保目录,作为晚期非小细胞肺癌的二线疗法使用,医保支付标准为510元(80mg/片)、300元(40mg/片),降幅达70%;2020年成功续签,一线及二线适应症全部纳入,有望进一步放量。
据药融云数据库,2022年,奥希替尼院内销售额达43.9亿元,是阿斯利康当之无愧的头号单品。
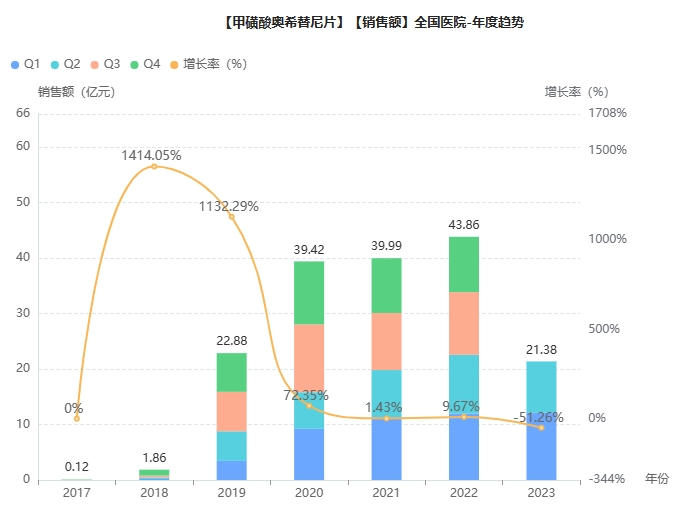
截图来源:药融云全国医院销售数据库
奥希替尼国内化合物专利CN103702990将于2032年7月到期,目前仅江苏万邦生化布局该仿制药。奥希替尼国内专利基本信息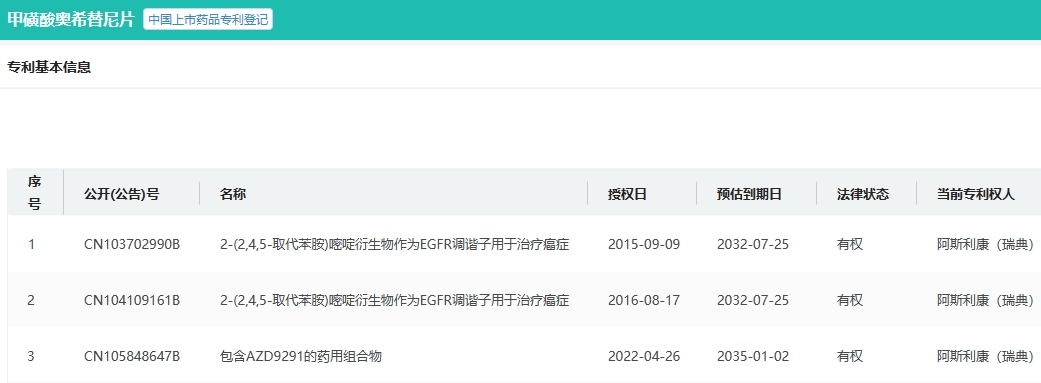
截图来源:药融云全球上市药品专利数据库
不过,面对奥希替尼所占领的庞大市场,依然有不少药企开展布局,陆续与奥希替尼开展头对头试验。
10月初,强生便宣布,其EGFR/c-MET双抗Rybrevant联合第三代EGFR抑制剂Lazertinib头对头奥希替尼治疗EGFR突变局部晚期或转移性非小细胞肺癌(NSCLC)患者的Ⅲ期MARIPOSA研究获得积极顶线数据。
2022年8月,EQRx和瀚森制药启动了阿美替尼的海外III期临床试验(TREBLE),对照组设置了阿美替尼+化疗组和奥希替尼组。但随着EQRx和翰森制药合作的中止,该研究的推进受到较大影响。
浙江同源康医药的TY-9591目前已完成Ⅰ期剂量爬坡和剂量扩展研究,正在开展一项对比奥希替尼一线治疗EGFRm+NSCLC患者的Ⅲ期临床研究,该研究(FLETEO)于2022年6月启动,计划招募680名患者。(登记号:CTR20221053)
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx