重磅大分子原研药和生物类似药的市场大战,如今明显提速!
近日,华东医药发布公告称,其全资子公司杭州中美华东制药近日提交了乌司奴单抗注射液(研发代码:HDM3001、QX001S)用于成年中重度斑块状银屑病的上市申请获得受理。

乌司奴单抗注射液是强生的重磅产品,于2009年在美国批准,2017年在中国上市,是针对性抑制IL-23及IL-12通路的首款生物药,也是全球治疗银屑病的主要疗法之一。2022年乌司奴单抗全球销售额高达97.23亿美元,2023上半年销售额达52亿美元,将有望在今年进入“百亿美元俱乐部”。
中美华东是首家提交乌司奴单抗生物类似药上市申请的国内药企。有业内人士指出,QX001S的上市或将率先打破乌司奴单抗原研品种在国内市场一家独大的销售格局,有望为临床患者提供更具经济性和可及性的国产替代选择;同时,作为重磅产品的生物类似药,也将为愈发激烈的生物类似药市场再加一把火。
首个国产乌司奴单抗抢占先机华东医药押宝皮肤赛道银屑病是一种慢性、复发性、炎症性疾病,主要累及皮肤和关节系统,目前尚无法治愈,需长期甚至终身治疗。目前治疗银屑病的方法有外用药物、系统治疗、物理治疗、生物制剂治疗等多种办法。由于银屑病的病程漫长、易复发,药物的长期疗效与安全性就显得尤其重要。国际银屑病共识认为,药物留存率作为银屑病的治疗目标之一,可以很好地反映药物的安全性、有效性及依从性。相较于传统治疗方案来说,以乌司奴单抗等为代表的生物制剂在治疗中重度银屑病时更高效、便捷,清除率也更高。
2017年强生的乌司奴单抗获批进入中国市场,目前在国内获批的适应症有成人斑块状银屑病、儿童斑块状银屑病及克罗恩病,2021年该产品顺利进入国家医保谈判目录。据米内网数据显示,2022年在中国三大终端六大市场乌司奴单抗的合计销售超过9.5亿元。在医保助力下,该产品2022年在中国公立医疗机构终端(城市公立医院、县级公立医院、城市社区中心及乡镇卫生院)的增长率达到1010.67%,已成为销售主战场。在零售药店终端(城市实体药店+网上药店),乌司奴单抗保持高速增长态势。
近年来快速增长的银屑病人数也促使这一领域市场规模快速扩容。根据弗若斯特沙利文的资料,2021年中国银屑病的患病人数为670万人,预计于2030年将达到690万,其中20%至30%的患者为中重度银屑病。2021年,中国的银屑病药物市场规模为11亿美元,预计于2030年将增长至95亿美元,复合年增长率为27.1%。其中,生物药2021年市场占有率为29.3%,随着国内庞大的患者群体和临床治疗需求,以及新药的不断进入,估计于2030年将上升至50.3%
行业普遍认为,广阔的市场前景,对于后来的国产乌司奴单抗而言,同样意味着巨大的机会。此外,今年原研药在中国市场的专利到期,也给了一众国内玩家后来居上的机会。
在皮肤、免疫领域,华东医药无疑是一个重要玩家。据2023年半年报,华东医药2023 年上半年实现营业收入203.85亿元,同比增长12.02%,若扣除股权激励费用及参控股研发机构等损益影响,实现扣非归母净利润 16.56 亿元,同比增长 20.61%。其中肿瘤、自身免疫、内分泌、医美、工业微生物以及医药商业六大矩阵筑牢了业绩底盘,源源不断地促进整体经营继续保持稳中向好态势。

在皮肤病领域,华东医药还引进了一款美国 Arcutis 公司全球创新的罗氟司特外用制剂(包括罗氟司特乳膏剂 ZORYVE和罗氟司特泡沫剂 ARQ-154),用以扩充自免领域外用制剂平台管线。目前 ZORYVE乳膏(0.3%)已在美国、加拿大上市,是首个也是目前唯一一个被批准用于治疗斑块型银屑病(包括间擦性银屑病)的局部外用 PDE4 抑制剂。
此外,华东医药的系统性红斑狼疮全球创新药 HDM3002(PRV-3279)Ⅱa 期临床试验申请也已获得 NMPA 批准。
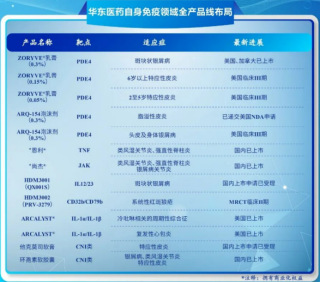
在生物类似药领域,华东医药还在今年大放异彩的GLP-1 赛道取得相当亮眼的成绩。华东医药以 GLP-1 靶点为核心,打造了全球领先的糖尿病创新药物研发平台,并建立了涵盖口服、注射剂等多种剂型包括长效和多靶点全球创新药和生物类似药相结合的 GLP-1 及相关靶点 8 个产品。2023 年上半年,华东医药利拉鲁肽糖尿病适应症和减肥适应症相继获批,均为国产首家,率先出线抢跑国内 GLP-1 市场。
生物类似药市场迅速扩容细分领域难逃激烈竞争
据不完全统计,国内生物类似药产品主要集中在阿达木单抗、贝伐珠单抗、利妥昔单抗、曲妥珠单抗等竞争激烈的单品领域,乌司奴单抗生物类似药的竞争目前较为缓和。
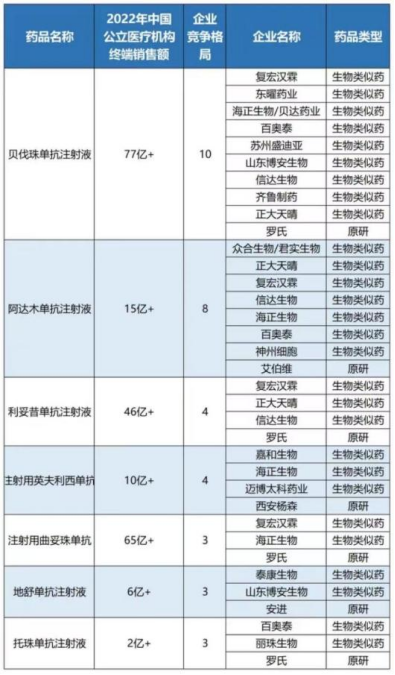
对于乌司奴单抗,首先出手的是安进。2022年4月,安进公布了乌司奴单抗生物类似药ABP 654一项III期临床研究初步结果,比较在中度至重度斑块型银屑病成人患者中开展,评估了ABP 654与Stelara的疗效和安全性。除安进外,Biocon Biologics、Alvotech、Celltrion等药企也已盯上了这片蓝海市场。今年1月,Alvotech及其销售合作伙伴Teva表示,FDA已经受理了他们的Stelara生物类似药上市申请,预计FDA将在2023年下半年完成监管审查。此外,韩国的Celltrion研发进程也走在全球前列,目前已进入临床三期,预计2024年左右进入市场。
面对强生创下的近百亿市场,国内药企也紧随其后。从在研格局来看,华东医药HDM3001进展最快,百奥泰和石药集团紧随其后,其布局的乌司奴单抗生物类似药也已分别推进至临床III期。
今年6月,百奥泰宣布与Biomm S.A.(以下简称“Biomm”)就BAT2206(签署授权许可及商业化协议。根据协议条款,Biomm将拥有BAT2206在巴西市场的独家分销权及销售权。据悉,BAT2206目前正在中国以及其它国家的患者中进行全球三期临床研究。百奥泰将计划向中国国家药品监督管理局(NMPA)、欧洲药品管理局(EMA)和美国食品药品监督管理局(FDA)递交上市申请。Biomm将负责巴西的上市申请递交。
此前,百奥泰还与英国药企 HikmaPharmaceuticals USA Inc. 达成合作,将乌司奴单抗生物类似药 BAT2206 在美国市场的独占商业化权益授权给 Hikama,获得 2000 万美元首付款 + 累计不超过 1.3 亿美元的里程碑付款和商业特许权使用费,以及两位数百分比的净销售额作为供货价。协议履行期限在美国市场首次商业化销售 BAT2206 之后 15 年届满。
石药集团是第三位杀入这一赛道的玩家。2022年6月,石药集团巨石生物首次公示其乌司奴单抗注射液的临床试验。目前,石药集团正在进行试验项目评估乌司奴单抗注射液与喜达诺治疗中度至重度斑块状银屑病有效性和安全性的多中心、随机、双盲、平行对照Ⅲ期临床试验。
进入21世纪以来,全球生物药产业快速增长,2020年全球生物类似药市场规模达到874亿美元;我国生物制药行业发展势头良好,与国际先进水平差距较小,在研生物药数量(临床前阶段)已经超越美国,居全球第一。如果持续抓住机遇跨越发展,大有机会实现赶超并确立引领地位。
据悉,中国在生物类似药上布局的企业已有近180家,其中代表性的企业有齐鲁制药、复宏汉霖、正大天晴、三生国健、双鹭药业、华兰基因、百奥泰、安徽安科生物、苏州康宁杰瑞、嘉和生物、信达生物、上海复旦张江生物等。中国生物类似药市场将于未来几年呈现爆发式増长,根据沙利文《中国生物类似药市场研究报告》中国生物类似药市场市场规模将于2030年达到589亿。



