连日来,资本市场“创新药”概念受到投资者热捧,医药板块的价值热度正在回归。
1月16日,绿叶制药早盘高开逾12%,截至收盘,涨幅达到4.04%,最终报4.27港元。
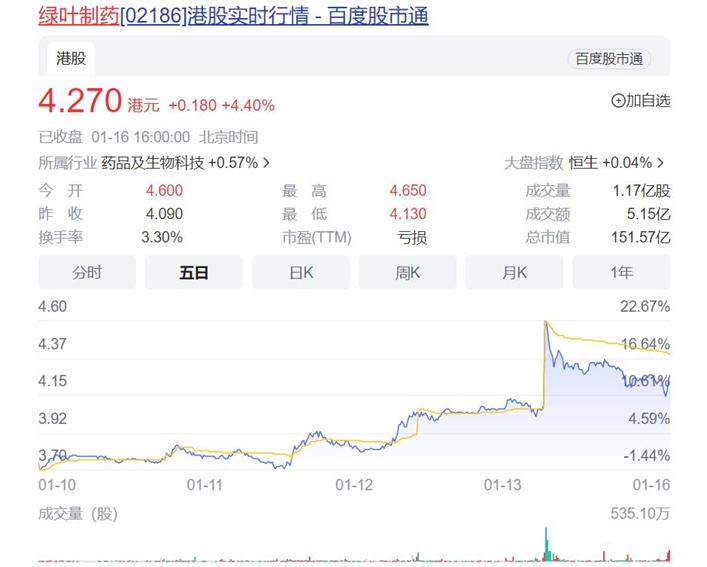
绿叶制药股价大幅跳涨,与创新药取得重要里程碑不无关联。1月16日,绿叶制药发布公告,公司自主研发的新药Rykindo (利培酮缓释微球注射制剂)正式获得FDA的上市批准。

中国创新药再次成功“出海”,无疑给过去一年冷清的二级市场医药板块带来了不少暖意。
更加值得关注的是,资本市场“创新药概念”持续走强,也让恒瑞医药的涨停更加受到投资者瞩目,全天超过49亿元的成交额,推动恒瑞医药市值重新逼近3000亿。

在业内看来,2021年以来医药板块下跌背后,一是因为过热的行业走势,其次则是集采杀价、出海不顺、疫情反复等市场情绪叠加。在长达一年的不断探底调整后,医药板块估值已经处于底部位置,新的投资机会逐步显现。
在走过寒潮低谷之后,资本市场“创新药”迎来全面反转?
505(b)(2)新药成功“出海”
国内改良型新药迎大爆发?
据了解,Rykindo是首个由中国药企自主研发并在美国获批上市的中枢神经系统治疗领域的新药,亦是首个根据联邦食品、药品和化妆品法案第505(b)(2)条款获得FDA批准上市的由中国大陆制药公司开发的复杂制剂产品。用于治疗精神分裂症成人患者、以及作为单药或作为锂盐或丙戊酸盐的辅助疗法用于双相障碍I型成人患者的维持治疗。
Rykindo的获批具有一定的里程碑意义。在业内看来,Rykindo获批意味着我国新药在该领域出海实现重大创新突破,表明全球监管认可中国在中枢神经系统治疗领域的新药研发能力,这不仅是绿叶制药“全球化战略”的又一重大成果,也是整个中国医药行业国际化的重要里程碑。
同时,505(b)(2)路径的创新药成功“出海”,或许意味着国内改良型新药将迎来大爆发。
除了绿叶制药,近年来,越来越多中国本土企业已经开始探索通过505(b)(2)途径进入美国市场,并且取得了不错的成绩。中国第一个通过505(b)(2)申报途径在美国FDA获批的NDA产品是石药集团的马来酸左氨氯地平片,于 2019年12月19日获批,用于降血压。第二个505(b)(2)改良型新药在美国FDA获批的是上海迪赛诺生物医药公司的产品多替拉韦钠拉米夫定替诺福韦片,于2020年10月6日获批,用于感染人类免疫缺陷病毒1型的成人和儿童的临床治疗。
从国内药企申报的情况来看,近年来,改良型新药研发主流趋势也正在加速酝酿,爆发期即将到来。
2021年,共有90多家企业申报了改良型新药。申报改良型新药最多的是恒瑞,共申报了38个。正大天晴、石药集团、越洋医药等企业的申报数量,都超过10个,尤其是越洋医药,其自主研发的30多个国际首创新药,在中美加印等国同步开展药物研究和临床试验。
2022年11月,齐鲁制药改良型新药利培酮口溶膜申报上市,用于治疗精神分裂症或双相情感障碍等。值得一提的是,在改良型新药方面,主攻口溶膜的齐鲁制药,在此前就已有5个口溶膜产品上市。
2022年10月,科伦药业2类改良型新药布瑞哌唑口溶膜获得临床实验默示许可,用于治疗成人患者的精神分裂症。目前,科伦药业主要有31款新药已处于申报临床及以上阶段,包括19款1类新药、9款2类改良型新药、3款生物类似药。
2022年9月,健康元发布公告称,收到国家药品监督管理局核准签发关于 XYP-001 的《药物临床试验批准通知书》,同意开展本品用于特发性肺纤维化的临床试验。XYP-001是一款健康元布局研发的改良型新药,拟用于治疗特发性肺纤维化(IPF)。
目前,为继续推动细分领域的市场发展,国家发布了一系列利好政策,如国家药监局在2020年就发布了《化学药品改良型新药临床试验技术指导原则(征求意见稿)》;2021年9月3日,在国家药品监督管理局的部署下,药审中心组织制定了《儿童用化学药品改良型新药临床试验技术指导原则(试行)》……
专家表示,505(b)(2)申报路径有很多优势,一是它是基于已经批准上市的药物进行的研究开发而提出的申请,有效降低了完全开发一个新药的失败率;二是可利用外部数据进行申报,并且可以通过桥接试验免除部分非临床或者临床试验,减少了相关费用,有效降低了成本;三是美国FDA给予新药3~7年的市场独占期。
业内认为,一系列政策正在鼓励创新制剂与改良型新药驶入快车道,创新药的重要性不言而喻,但改良药的临床价值和市场价值也同样值得重视。通过505(b)(2)申报路径进行NDA逐渐成为中国本土企业中美双报的路径之一,未来还将会有更多的企业通过此途径进行申报。
二级市场持续走强
“创新药概念”全面回暖?
随着我国创新药技术整体持续提高,与国际水平逐步缩小,将支撑改良型新药行业增长。根据NMPA官网公示,2022年已经有超过50款新药(不完全统计)在中国获批上市,获批产品数量继续保持高速增长。
近年来,受资本市场的投资情绪影响,市场板块轮动、估值压制以及地缘因素等综合因素,医药板块经历了接近5个季度的熊市,申万医药指数从2021年7月初的高点到2022年9月底的低点,跌幅超40%,接近腰斩。
经历了漫长的底部出清后,2022年下半年多个新出台集采政策均显示出边际放缓的变化,一次次的集采全部指向共同的趋势:未来集采会趋向温和,价格的降幅相对可控。叠加对医疗和科研设备贴息贷款、业绩增长得到验证等利好,医药板块在漫漫熊市途中迎来了转折向上的关键催化。
1月16日,以恒瑞医药为代表的创新药板块持续走强,高开高走,最终以9.83%,报43.13元收盘,股价创本轮反弹新高,市值定格在2751亿元,距离重返3000亿元只有一步之遥。
数据上看,恒瑞医药近3日累计涨幅12.35%,近5日累计涨幅9.23%,前3日主力资金累计净流入1.36亿元;前5日主力资金累计净流入1.36亿元。
同日,恒瑞医药公布,近日,江苏恒瑞医药股份有限公司子公司山东盛迪医药有限公司收到国家药品监督管理局下发的《受理通知书》,公司提交瑞格列汀二甲双胍片(HRX0701片)的药品上市许可申请获国家药监局受理。
HRX0701片是公司开发的二肽基肽酶IV(DPP-4)抑制剂磷酸瑞格列汀与盐酸二甲双胍固定剂量复方制剂,通过两种不同作用机制达到更好的降血糖作用。据悉,截至目前,HRX0701片相关项目累计已投入研发费用约2208万元。
与国内头 部规模较大的创新药企业相比,恒瑞的研发投入体量及研发投入增速均处于领先地位。2018 年至 2021 年,恒瑞医药研发投入从 26.7 亿元增长至 62.03 亿元,研发投入占营收比例从 15.3%增长至 24%。2021 年起,公司对部分 III 期临床研发 费用进行了资本化处理,研发费用仍然达到 59.4 亿,研发费用率达到 22.9%。
2022年上半年恒瑞医药累计研发投入达到29.09亿元,同比增加12.74%,研发投入占销售收入的比重同比提升至28.44%,创历史新高。
在大规模研发投入下,恒瑞医药创新药取得丰富成果。2022年上半年,恒瑞医药在研创新药达60多个,在国内外开展260多项临床研究。创新药临床试验进度加快,自主研发的AR抑制剂瑞维鲁胺片获批上市,已上市创新药增至11款,位居国内同行业前茅。
有业内人士表示,随着恒瑞医药研发投入持续增长,创新药加速放量在即,经营拐点渐现。加上疫情防控的优化,社会活动开始逐步恢复正常,医院也将恢复正常的诊疗活动,2023年医药板块也将迎来全面复苏。
从估值角度来说,医药板块经历2021-2022年多轮调整后,绝大部分子板块2023年预期市盈率都处于2017年来低位。因此2022年4季度和今年的1季度非常关键,是医药企业拐点的关键季度,如果确认了拐点,2023年业绩甚至股价值得期待。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx