9月7日,礼来递交的「替尔泊肽注射液」5.1类进口申请获CDE受理。替尔泊肽(Tirzepatide)是一种每周一次的葡萄糖依赖性促胰岛素多肽(GIP)受体和胰高血糖素样肽-1(GLP-1)受体双重激动剂,今年5月被FDA批准作为饮食和运动的辅助手段,以改善成人2型糖尿病患者的血糖控制,商品名Mounjaro。
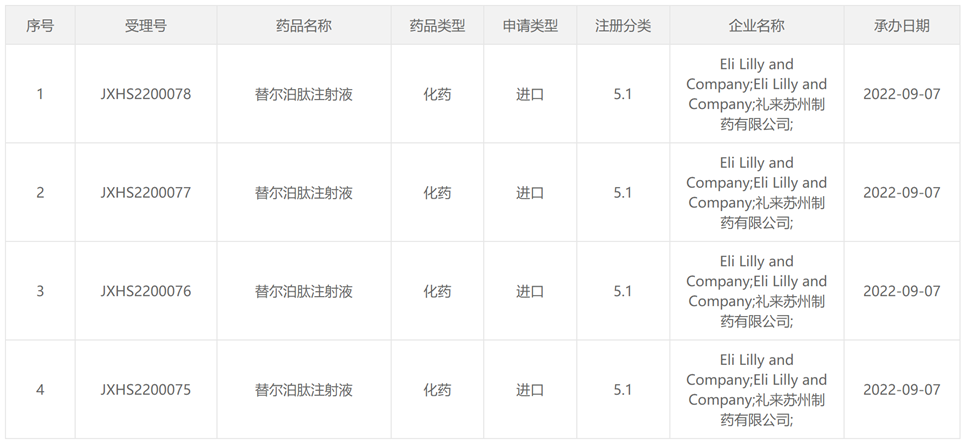
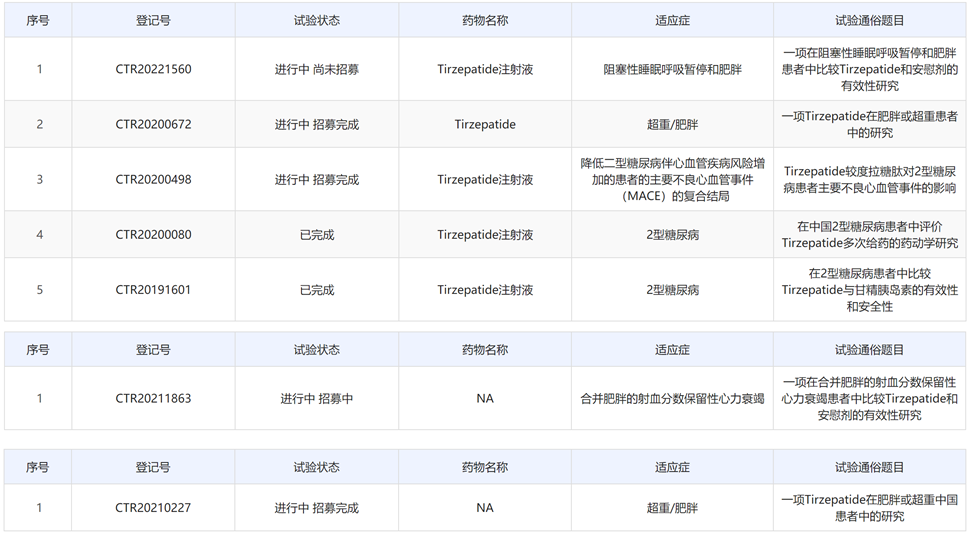
据CDE药物临床试验登记与信息公示平台,Tirzepatide在国内共登记7项临床试验,适应症涉及2型糖尿病、超重/肥胖、阻塞性睡眠呼吸暂停和肥胖和合并肥胖的射血分数保留性心力衰竭等。据临床试验进度,笔者推测此次Tirzepatide申报的适应症为2型糖尿病。
治疗2型糖尿病方面,今年1月礼来宣布Tirzepatide在为期40周的SURPASS-AP临床试验(将Tirzepatide与剂量滴定的甘精胰岛素进行比较)中达到主要和所有关键性次要终点,显著降低2型糖尿病患者的糖化血红蛋白和体重。
SURPASS-AP是一项国际多中心III期临床试验,旨在在接受稳定剂量的二甲双胍治疗(联合或不联合磺脲类药物)血糖仍控制不佳的2型糖尿病患者中,比较接受三种不同剂量的Tirzepatide(5 mg,10 mg和15 mg)和剂量滴定的甘精胰岛素治疗的有效性和安全性。
试验结果显示:与对照组甘精胰岛素相比(40周时的平均剂量为每天25.4单位),不同剂量的Tirzepatide(5 mg,10 mg和15 mg)均实现糖化血红蛋白和体重的显著降低,且三个剂量组中,高达86%的患者达到糖化血红蛋白低于7%(中华医学会糖尿病学分会建议的控制目标)。
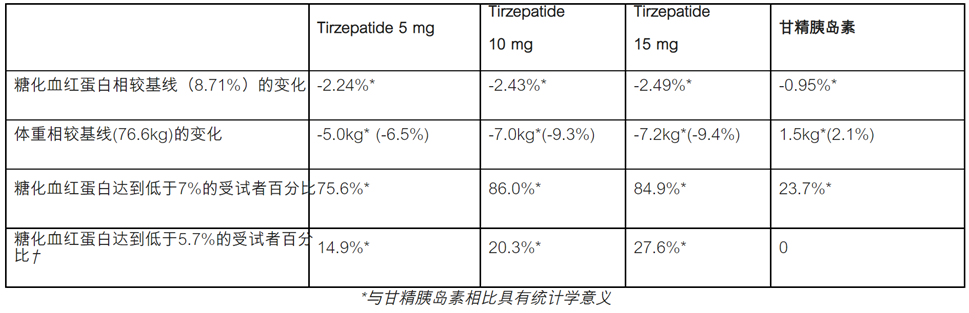
图片来源:礼来官网
安全性方面,Tirzepatide的总体安全性与先前报道的SURPASS系列试验相似,其中轻中度胃肠道反应是最常见的不良反应,并随着持续给药而降低。而且,试验中Tirzepatide三个剂量组中低于 3.9 mmol/L(70 mg/dL)的低血糖发生率均显著低于甘精胰岛素组。
SURPASS-AP试验结果用以支持Tirzepatide在中国等亚太地区2型糖尿病适应症申请,期待未来Tirzepatide可以早日在国内获批上市,造福广大2型糖尿病患者。
此外,Tirzepatide在减重方面的实力也不容小觑。今年4月,礼来宣布Tirzepatide治疗肥胖症或超重群体的全球III期临床试验SURMOUNT-1取得积极结果。该试验是Tirzepatide在肥胖患者中开展的第一项全球多中心、随机、双盲、平行、安慰剂对照试验,共入组2539名伴有至少一种疾病(高血压、血脂异常、阻塞性睡眠呼吸暂停综合征或心血管疾病,但不伴有糖尿病)的肥胖或超重患者,试验中受试者按1:1:1:1分组接受5mg、10mg、15mg的Tirzepatide或安慰剂治疗,以评估在低卡路里饮食和增强运动基础上添加使用Tirzepatide与安慰剂的减重疗效和安全性差异。
结果显示:Tirzepatide (5mg、10mg、15mg)治疗组患者第72周时减重效果均显著优于安慰剂对照组,同时接受最高剂量(15mg)tirzepatide治疗的亚组平均体重降低22.5%(约24公斤),其中63%的受试者体重降低至少20%。值得一提的是,Tirzepatide是在3期临床试验中首 个将体重平均降低超过20%的在研药物。
肥胖和糖尿病一样,患者体量非常庞大。如果说糖尿病市场太过拥挤,肥胖症市场有望成为Tirzepatide走上巅峰的一大助力。据悉,目前在肥胖症市场已获批的类似机制药物有限,已获批的GLP-1受体激动剂仅有诺和诺德的利拉鲁肽和司美格鲁肽。其中利拉鲁肽于2014年12月被FDA批准,商品名为Saxenda,其III期临床结果显示,60%的肥胖症患者注射利拉鲁肽后体重下降5%,1/3患者体重的降幅能达到10%。司美格鲁肽于2021年8月被FDA批准,商品名为Wegovy,其IIIa期阶段的4项临床试验数据显示,每周皮下注射1次2.5mg司美格鲁肽,减重在16.9%-18.2%。
业界人士表示,以往上市的减肥药多数减重效果徘徊在5%-10%的区间,且副作用大、连续性差,如果能减重15%以上将非常具有市场前景。从已公布的试验数据看,Tirzepatide和司美格鲁肽将在减重市场上演神仙打架。目前,诺和诺德已率Saxenda和Wegovy两款产品率先入局,且已取得不错成绩。据悉这两款产品2021全年销售额高达84亿丹麦克朗,而今年上半年这两款产品销售额就高达70.45亿丹麦克朗,其中Saxenda 2022H1销售额为25.85亿丹麦克朗,Wegovy 2022H1销售额为44.60亿丹麦克朗。Wegovy上市后的碾压式表现着实惊艳。
除了疗效,定价也是影响患者选择的一个重要因素。据悉,目前Tirzepatide(Mounjaro)在美国的定价为每月(4支)约974美元,而Wegovy定价为每月1349美元,Saxenda 定价为每月约1000美元。虽然Mounjaro还未被批准用于减重,但富国银行分析师Mohit Bansal表示其较低的定价可能为标签外使用打开大门。
此外,Tirzepatide还有望成为射血分数保留的心力衰竭(HFpEF)、非酒精性脂肪性肝炎(NASH)等疾病的潜在疗法。业绩非常看好Tirzepatide,Evaluate Vantage曾预测其2026年销售额有望达到49亿美元,不过业界分析师们认为普遍低估Tirzepatide的潜力,美国硅谷银行(SVB)认为其2030年销售额可能达到141亿美元。
不过新药研发竞技场上没有永远的王 者,目前在2型糖尿病、减重市场还有很多不可小觑的后浪,如信达生物的GLP-1/GCGR双靶点激动剂Mazdutide (IBI362)、SCOHIA PHARMA/华东医药的 GLP-1R/GIPR双靶点激动剂SCO-094、勃林格殷格翰的GLP-1/GCGR双靶点激动剂BI456906、安进的GLP-1R/GIPR双靶点激动剂AMG133。
版权所有,未经允许,不得转载。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx