5 月 18 日,中国生物制药宣布子公司正大天晴已与 Symphogen A/S 签订协议,获得
LAG-3 单克隆抗体 Sym022 的全球权益。Symphogen 是施维雅的全资子公司及抗体重点研发中心。
Sym022 是全人源重组的 LAG-3 单克隆抗体,且在临床前阶段展现出了良好的肿瘤抑制潜力。目前该产品已完成了两项临床 I 期实验,临床结果显示其不论是作为单独用药或者是联合其他肿瘤免疫检查点抑制剂用药都具有良好的安全性和耐受性。
Sym022 全球研发进度甘特图
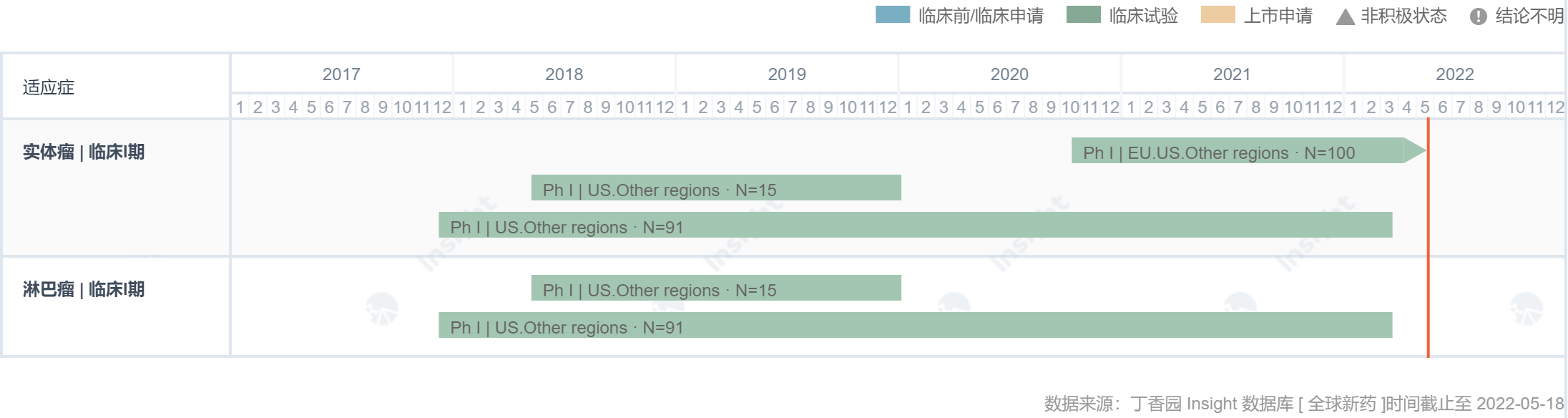
来自:
Insight 数据库全球新药模块(http://db.dxy.cn/v5/home/)
目前这笔交易涉及金额尚未披露,预计在 6 月份将完成交割。LAG-3 单抗作为已获临床验证的肿瘤免疫靶点,可与天晴的 PD-1 派安普利单抗(安尼可®)、PD-L1 单抗 TQB2450、TIM3 单抗 TQB2618、安罗替尼等药物联合用药,进而加强天晴对肿瘤领域的深度开发。
LAG-3 是继 PD-1、CTLA-4 之后全球第 3 个实现商业化的免疫检查点,已经在 PD-1 联合疗法中表现出优异疗效。今年 3 月,百时美施贵宝 First-in-class 双免疫疗法
Relatlimab + Nivolumab 固定剂量组合 Opdualag 获 FDA 加速批准上市,治疗转移性黑色素瘤,在标准治疗方案 O+Y 组合之外为黑色素瘤患者提供了新的治疗方案;针对其他实体瘤,BMS 也展开了广泛的开发。
相较于 CTLA-4,LAG3 在安全性上潜在更具优势。Opdualag 的关键临床研究 RELATIVITY-047 研究中,LAG3 组合的 12 个月 PFS 数据与 O+Y 组合相似,而严重副作用的发生率仅 19%,远低于 O+Y 组合的 59%。不过 LAG3 组合疗法的临床数据相对不如 O+Y 方案成熟,因此还待更长期的数据来展现最终为患者带来的获益情况。
据 Insight 数据库 全球新药数据显示,当前已有 50 个 LAG3 抗体药项目在研,其中 27 款已经进入到临床开发阶段,包括 18 个单抗,7 个双抗,2 个单抗复方。根据它们结合 LAG3 的位置,这些抗体可能具有不同的能力来阻断 LAG3 及其各种配体的相互作用。
临床阶段 LAG3 抗体药类别分布
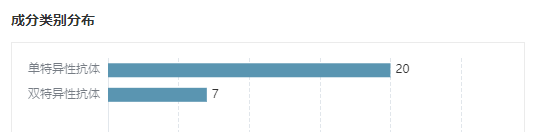
来自:
Insight 数据库 全球新药(http://db.dxy.cn/v5/home/)
目前,LAG3 抗体主要以 PD-1 联用的形式开发,拥有 K 药和 O 药两大超级重磅炸弹的默沙东和百时美施贵宝借免疫疗法赛道的先发优势继续跑在最前方。BMS 率先取得了首项批准,而
默沙东的 MK-4280A 也已经在 2021 年 9 月首次启动 III 期临床,用于 PD-L1 阳性结直肠癌。
再生元/赛诺菲的 fianlimab 处于第 3 位,4 月 6 日针对黑色素瘤也启动了 III 期临床。
而把目光放到国内,据
Insight 数据库,中国企业参与开发的 LAG-3 抗体药已有 19 个,其中 12 个项目为单抗,进展阶段如下图。
已有 PD-(L)1 单抗报批的企业中,恒瑞、信达、百济、复宏汉霖、誉衡、科伦……均有 LAG-3 单抗项目在研。本次通过引进 LAG3 单抗,正大天晴此次也加入了这一行列的竞争。
中国企业的 LAG3 单抗研发状态分布
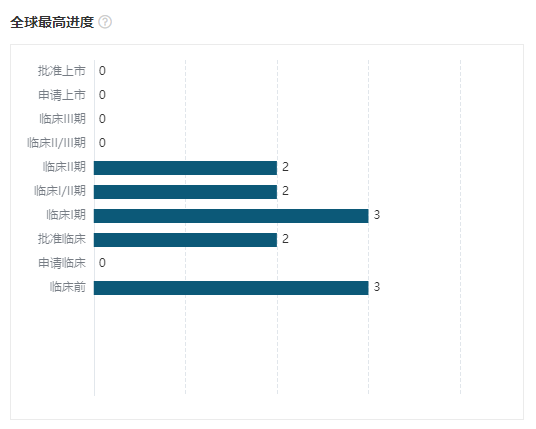
来自:
Insight 数据库 全球新药(http://db.dxy.cn/v5/home/)
从趋势来看,LAG3 靶点项目申报自 2019 年开始迸发,2021 年达到小高峰,当前共有 15 个项目已经进入临床开发阶段,包括 10 个国产和 5 个进口。国内 LAG3 项目研发趋势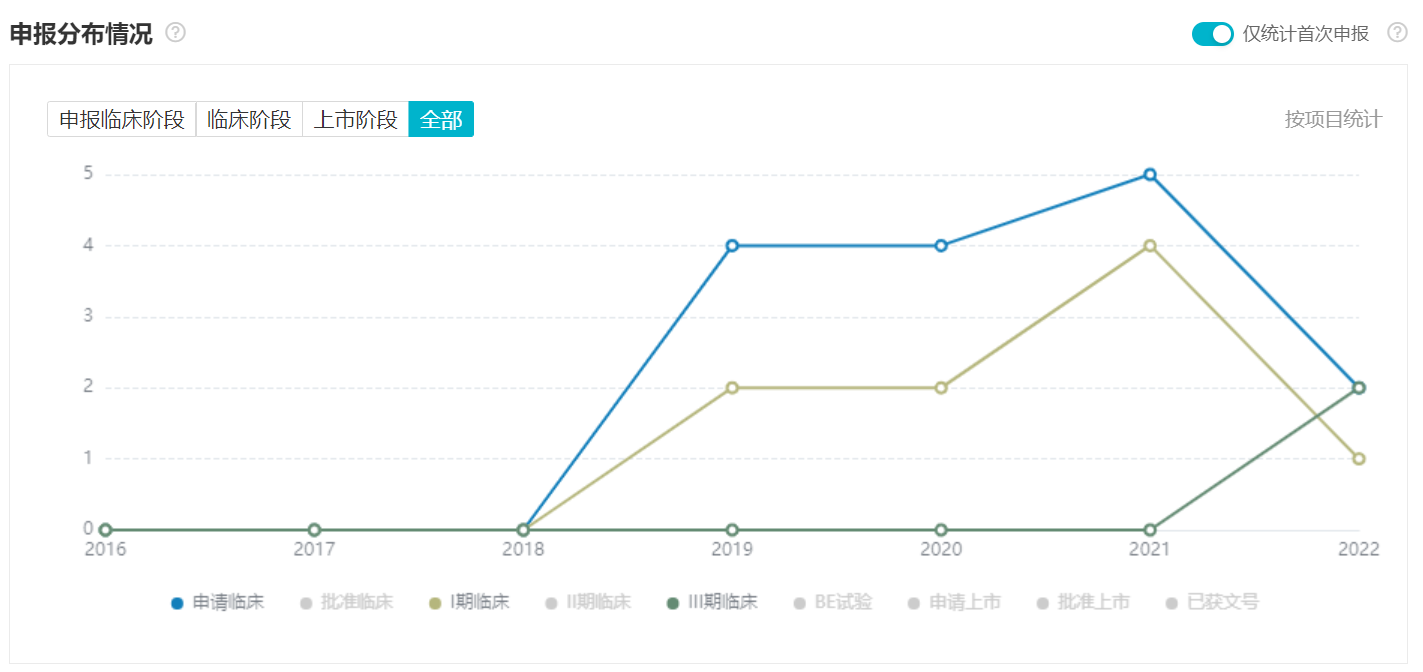 来自:Insight 数据库 项目进度(http://db.dxy.cn/v5/home/)信达生物是唯一一家单抗、双抗均进入临床的企业,LAG3 单抗 IBI110 已经启动 II 期临床,PD-L1/LAG3 双抗 IBI323 正处于 I 期临床阶段。进入 II 期临床的项目还包括 3 款 LAG3 单抗:恒瑞医药的 SHR-1802、百济/维立志博的 LBL-007、时迈药业的 DNV3。
来自:Insight 数据库 项目进度(http://db.dxy.cn/v5/home/)信达生物是唯一一家单抗、双抗均进入临床的企业,LAG3 单抗 IBI110 已经启动 II 期临床,PD-L1/LAG3 双抗 IBI323 正处于 I 期临床阶段。进入 II 期临床的项目还包括 3 款 LAG3 单抗:恒瑞医药的 SHR-1802、百济/维立志博的 LBL-007、时迈药业的 DNV3。
国内处于 II 期临床的 LAG3 单抗
来自:
Insight 数据库 项目进度(http://db.dxy.cn/v5/home/)
从 3 月份数据来看,PD-(L)1 之后的几大免疫检查点之中 TIGIT 是头号热门,LAG3 紧随其后,两者都是前期阶段项目储备众多,蓄势待发。LAG3 单抗成功获批上市,而 TIGIT 则接连遭遇两次挫折。后续赛道热度是否会有变化?还待时间来证明。
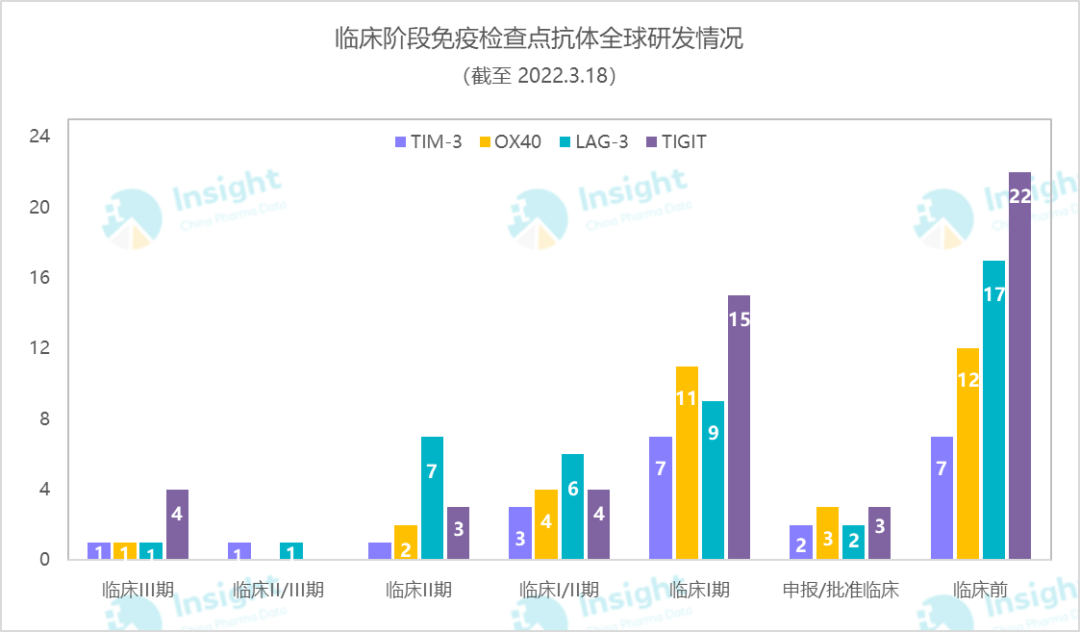
 来自:Insight 数据库全球新药模块(http://db.dxy.cn/v5/home/)
来自:Insight 数据库全球新药模块(http://db.dxy.cn/v5/home/) 来自:Insight 数据库 全球新药(http://db.dxy.cn/v5/home/)
来自:Insight 数据库 全球新药(http://db.dxy.cn/v5/home/) 来自:Insight 数据库 全球新药(http://db.dxy.cn/v5/home/)
来自:Insight 数据库 全球新药(http://db.dxy.cn/v5/home/) 来自:Insight 数据库 项目进度(http://db.dxy.cn/v5/home/)
来自:Insight 数据库 项目进度(http://db.dxy.cn/v5/home/) 来自:Insight 数据库 项目进度(http://db.dxy.cn/v5/home/)
来自:Insight 数据库 项目进度(http://db.dxy.cn/v5/home/)