在继恒瑞在 2019 年 9 月递交卡瑞利珠单抗用于非鳞状非小细胞肺癌(NSCLC)一线治疗上市申请后,今年 4 月 21 日和 24 日,百济神州和信达先后递交了 PD-1 抗体药物替雷利珠单抗和信迪利单抗,用于鳞状 NSCLC 和非鳞状 NSCLC 一线治疗的新适应症上市申请。
就在今天(5 月 7 日),信达宣布信迪利单抗联合疗法一线治疗鳞状 NSCLC 的 III 期临床达到主要终点,将于近期沟通递交新适应症上市申请。至此,国产 PD-1 抗体药物开始进入了 NSCLC 一线治疗的竞争赛道。
国产 PD-1 抗体药物已批准和正在审评适应症

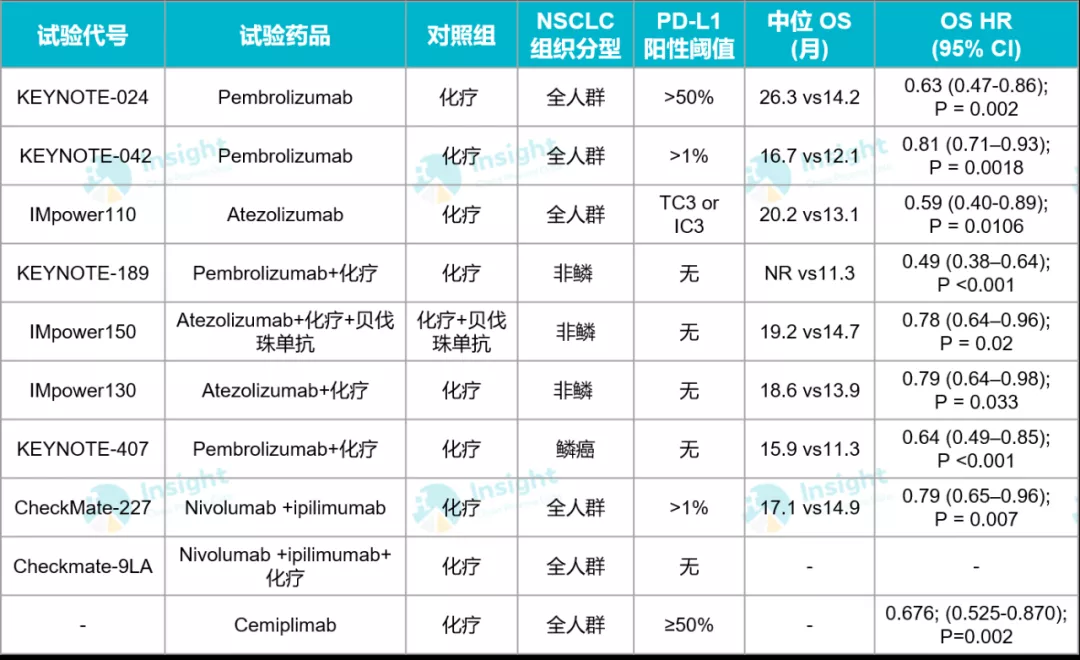
国产 PD-1 抗体药物晚期 NSCLC 一线治疗结果

PD-1 抗体药物改善 NSCLC 一线治疗生存格局
纳武利尤单抗(Nivolumab) 在 2015 年 3 月是最早拿下 NSCLC 二线用药的 PD-1 抗体药物,但随后就被帕博利珠单抗(Pembrolizumab) 在二线和一线治疗领域逆袭和建立了难以突破的优势。
2001 年, 含铂双药方案成为晚期 NSCLC 一线化疗的标准,一年生存率大概为30-40%,总生存 OS 约为 12 个月,这一治疗标准从2016 年的 KEYNOTE-024 试验开始有了很大的改变,Pembrolizumab 在肿瘤细胞PD-L1 表达≥50% 的 NSCLC 中 OS 突破至前所未有的 26 个月,使得 Pembro 在 2016 年成为第一个获批用于晚期 NSCLC 一线治疗的 PD-1 抗体药物。
在随后的 KEYNOTE-042 试验中也显示,PD-L1 表达≥1% 的 NSCLC 患者人群也显示生存获益。IMppower110 试验中也比较了 PD-L1 抗体药物阿替利珠单抗 (Atezolizumab) 与化疗相比,在肿瘤或肿瘤浸润免疫细胞(TC3 或 IC3)PD-L1 表达≥50% 的 NSCLC 显示生存获益,也可能再为一线治疗提供新选择。目前这一人群随着赛诺菲的 cemiplimab 宣布 III 期试验的成功而准备迎来新竞争者。
约有 30% 的晚期肺癌患者中 PD-L1 表达>50%,而对于非高表达患者,我们仍期望免疫治疗能够带来获益,于是探索了免疫联合化疗的治疗模式。Pembrolizumab 的 KEYNOTE-189 试验,确定了对于无论 PD-L1 表达人群,PD-1 抗体+化疗相比化疗作为一线治疗显示 PFS 和 OS 的显著获益,基于此试验在 2018 年 8 月获得了 FDA 的批准。Atezolizumab+化疗±贝伐珠单抗在 Impower150 和 Impower130 试验中都显示了生存获益,为非鳞 NSCLC 患者提供一线治疗更多选择,于 2018 年 12 月这一「豪华版」用药组合获批该适应症。
对于占比 30% 的鳞癌 NSCLC 患者,Pembrolizumab 的 KEYNOTE-407 一线治疗试验显示了生存获益,并在 2018 年 10 月在 FDA 获批此适应症。尽管如此,NSCLC 患者的预后仍然需要提高,在 KEYNOTE-189 和 KEYNOTE-407 试验中,有约 65% 和 70% 的患者治疗一年后疾病进展。虽然 Pembrolizumab 加化疗在鳞癌以及非鳞癌中都可以显著延长 OS,但是在非鳞癌似乎更加有效(0.49 vs 0.64)。
PD-(L)1抗体药物在 NSCLC一线治疗探索之路
双免疫疗法在 NSCLC 探索一波三折
双免疫疗法在 NSCLC 一线治疗被寄予厚望,BMS 希望通过设计非常复杂的 CheckMate-227 试验打入 NSCLC 一线治疗,但这个复杂试验过程颇为波折。
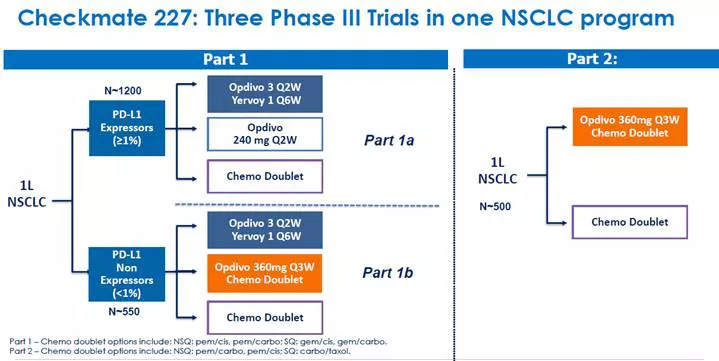
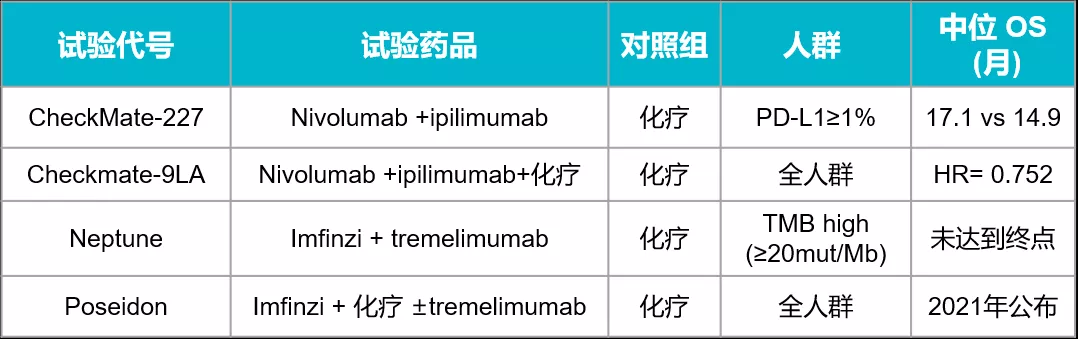
根据已经公布的试验结果,Part1 试验是探索 Nivo+Ipi 对比化疗在 PD-L1 表达≥1% 和<1% 的的生存获益,但仅显示在 PD-L1≥1% 的患者中显著提高 OS,且押注的 TMB 在 NSCLC 中没有显示可以成为一个好的生物标记物,Nivo+Ipi 联用在 TMB 高表达和低表达人群都显著提高,所以 BMS 在欧盟撤回了基于这一试验在高 TMB 水平 NSCLC 一线治疗的上市申请。此前,AZ 纳入 TMB ≥20mut/Mb 人群的 Neptune 试验也在在 2019 年宣告失败;Part2 试验主要是探索 Nivo+化疗用于非鳞 NSCLC 一线治疗,最终结果显示与化疗相比,OS 没有显著提高(18.8 vs. 15.6mos, HR=0.86,P=0.1859)。
目前看 Nivo+Ipi 与 Pembrolizumab 单药在 PD-L1≥1% 的 NSCLC 人群 OS 类似,但毒性有所增加。2020 年 1 月美国 FDA 根据 CheckMate-227 Part1 试验结果对 N+I 一线治疗 NSCLC 进行优先审评, NSCLC 一线治疗有希望进入「去化疗」的新里程碑。
在 CheckMate-9LA 试验 Nivo+Ipi+有限疗程含铂双药化疗达到主要终点后,2020 年 4 月 8 日,FDA 此三药联用组合用于无论 PD-L1 表达的晚期 NSCLC 一线治疗申请。
CTLA-4+PD-1 抗体药物用于 NSCLC 的关键性试验
国内 PD-(L)1 抑制剂 NSCLC 试验竞争激烈
因肺癌是全球发病率和死亡率最高的癌症,肿瘤市场向来有「得肺癌者得天下」的说法,Keytruda 自 2016 年首先拿下 NSCLC 一线治疗市场后,销量一路快速上升,在美国市场的销售收入约有 65% 来源于肺癌,Tecentriq 在 2018 年 12 月获批了一线治疗 NSCLC 的适应症,从 2019 年开始销量也有了一个明显的增长。
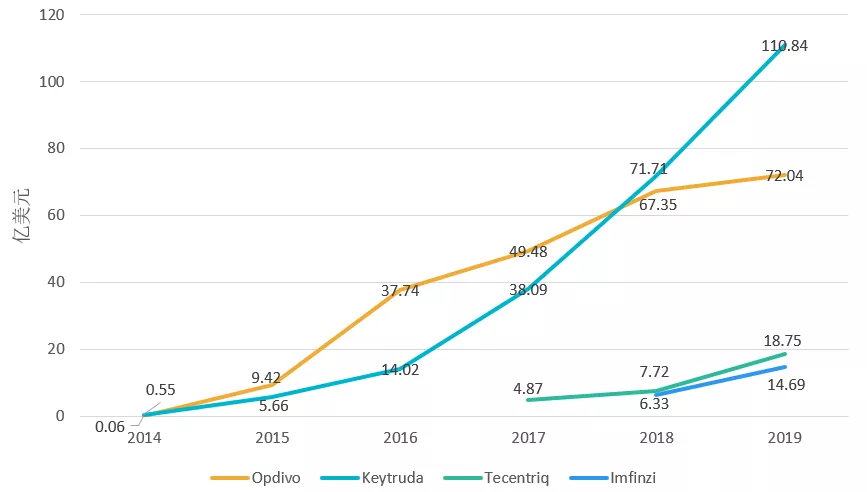
4 款 PD-1/PD-L1 药物年销售额(亿美元)
不仅国际市场上 PD-(L)1 抑制剂将进入 NSCLC 一线治疗白热化竞争,国内市场也是,目前正在进行的用于 NSCLC 生物药靶点中 PD-(L)1 抑制剂数量最多,君实、基石、康方、复宏汉霖、神州细胞、正大天晴等都进入了 III 期。另外 3 个包括 PD-(L)1 靶点在内的「升级版」双抗产品均进入了 II 期阶段,包括与 Pembrolizumab 进行头对头的 TGFβR/PD-L1 双功能融合蛋白 M7824,国内两家双抗龙头药企康方和康宁杰瑞的 AK104 和 KN046。
除此之外 VEGF 抑制剂肺癌市场竞争也相当激烈,在 2019 年 12 月齐鲁成为首个获批的 VEGF 抑制剂贝伐珠单抗生物类似药,用于非鳞 NSCLC 和结直肠癌,信达和恒瑞也都先后提交了 NDA,处于 III 期临床阶段的分别是东曜药业、天广实、百奥泰、嘉和生物、博安生物、复宏汉霖、正大天晴、华兰基因、神州细胞和安科生物,除复宏汉霖开展了非鳞 NSCLC 和结直肠癌 2 个临床试验外,其他均只开展非鳞NSCLC临床试验。
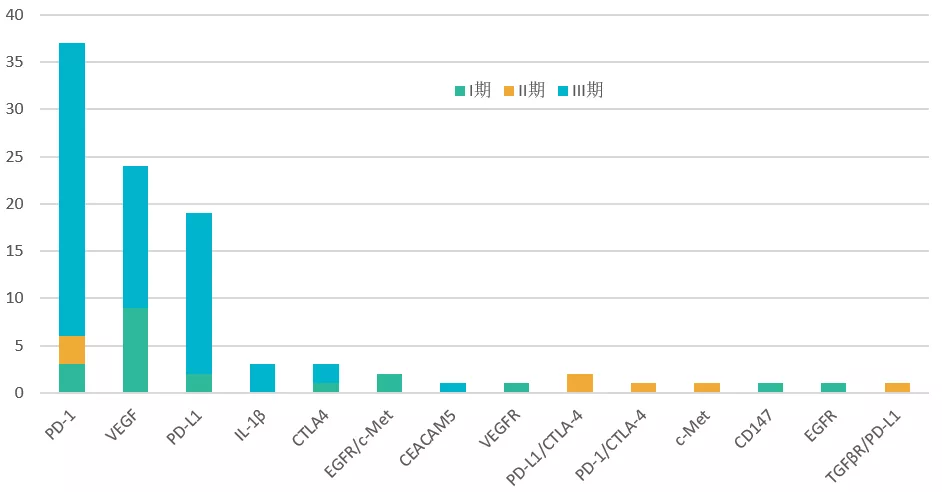
国内正在进行 NSCLC 临床试验的生物药靶点分布
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx