12月27日,百济神州替雷利珠单抗注射液的上市申请(CXSS1800019)获得国家药监局批准,用于治疗复发难治性经典型霍奇金淋巴瘤( r/r cHL)。这是中国获批上市的第6款PD1药物。
百济还在开展10多项关于替雷利珠单抗的注册临床试验,适应症包括非小细胞肺癌、肝细胞癌、食道鳞状细胞癌、胃癌和鼻咽癌等。百济在2019Q3财报中预计其替雷利珠单抗将于2020年在中国获批第2项适应症,即治疗局部晚期或转移性尿路上皮癌(UC)患者。除此之外,替雷利珠单抗预计的里程碑事件还有:

全球目前已有10款PD-1/PD-L1药物获批,来自中国的有4款。截至目前,已经有7款PD-1/PD-L1药物在中国上市,r/r cHL成为最为拥挤的适应症。
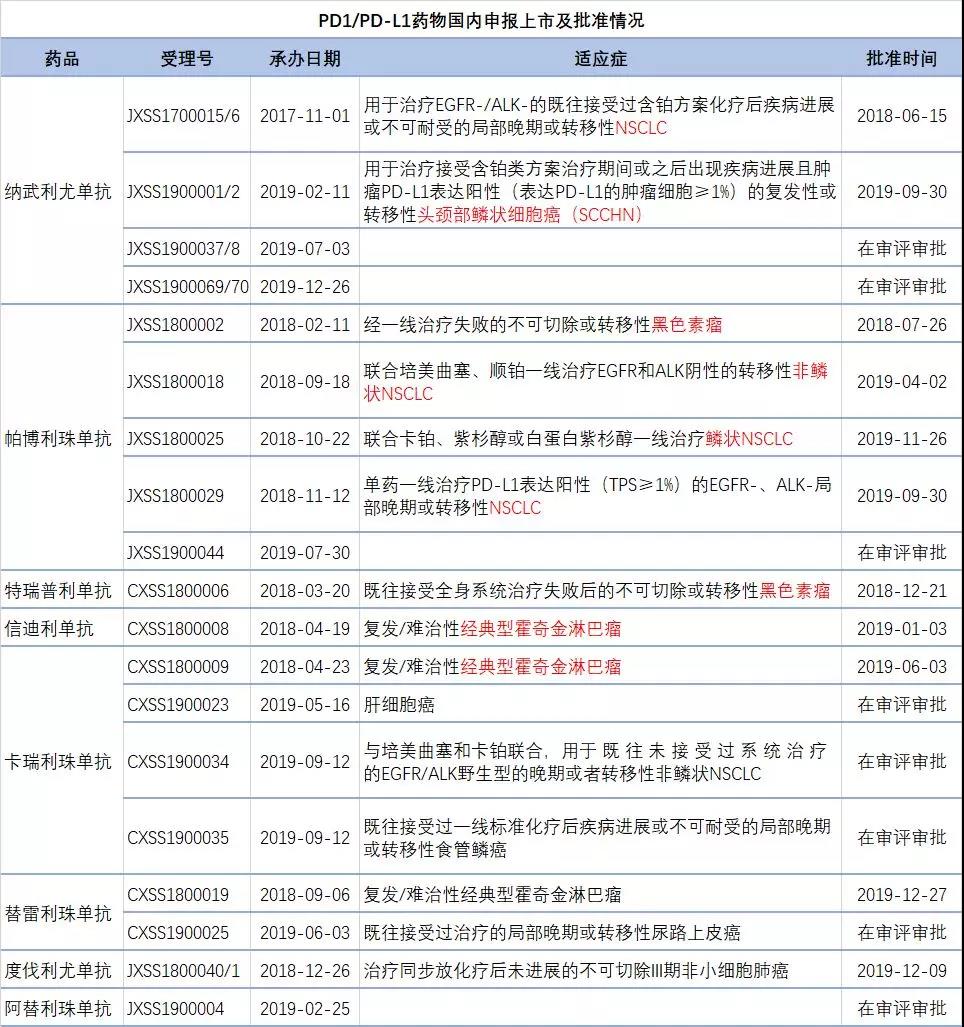
目前,信达生物的信迪利单抗已以63.73%的降幅,2843元(10ml:100mg/瓶)的价格进入国家乙类医保,成为唯一一个入选2019年国家医保谈判药品名单的PD-1,限至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤的患者。协议有效期为2020年1月1日至2021年12月31日。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx