摘要
12月CDE共承办药品注册申请791件
66个一致性评价品种获CDE承办,其中18个品种为首家申报
7个品种有首家企业提交仿制申请
4个1类新药获批,19个新注册分类仿制药获批
20个品种有企业通过一致性评价
91个品种获临床试验默示许可
CDE总体承办情况
据MED中国药品审评数据库2.0统计,2019年12月CDE共承办药品注册申请791个。除新药申请和进口申请外,仿制申请和一致性评价申请比上月均有所上升。
2019年CDE承办药品注册申请情况(按受理号计)
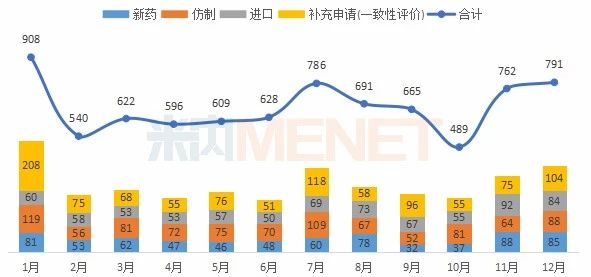
一致性评价补充申请承办情况
12月有66个药品的一致性评价补充申请获CDE承办(11月为48个),其中口服制剂有37个,注射剂有29个,有18个品种首家企业开始一致性评价。详细情况请见下表:
2019年12月CDE补充申请(一致性评价)口服制剂品种承办情况
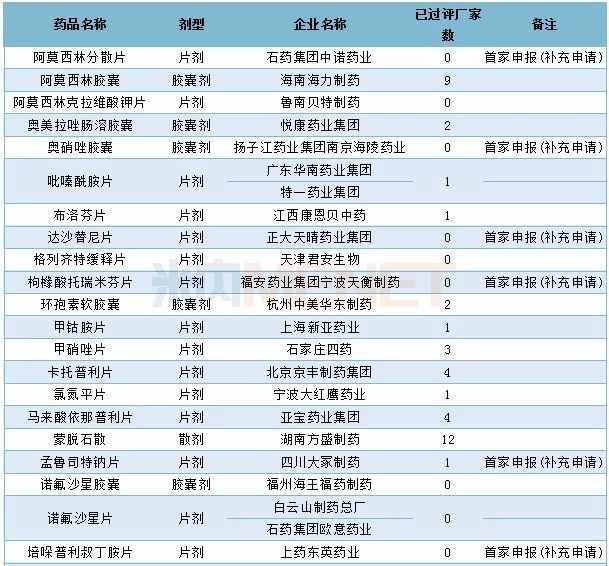
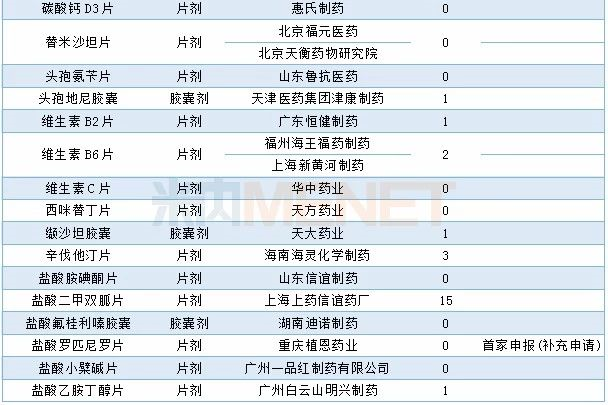
2019年12月CDE补充申请(一致性评价)注射剂品种承办情况
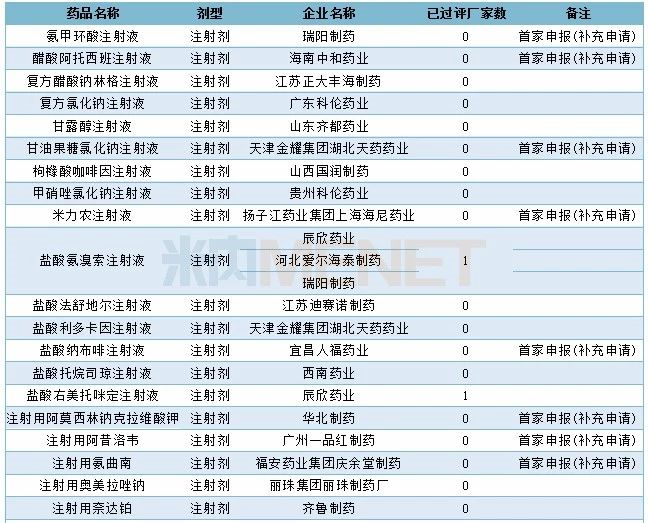
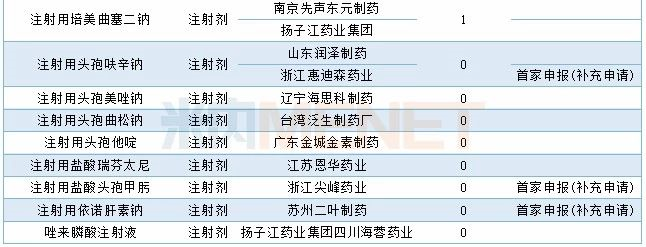
(说明:仅统计以补充申请申报的一致性评价受理号,过评情况按药品名称统计)
新药申请承办情况
12月有51个药品的新药申请获CDE承办,其中属于1类新药的有28个,2类改良型新药(2.2类、2.4类)6个。此外还有5个中药新药,其中昆明邦宇制药的小儿脾胃乐颗粒为上市申请。详细情况请见下表:
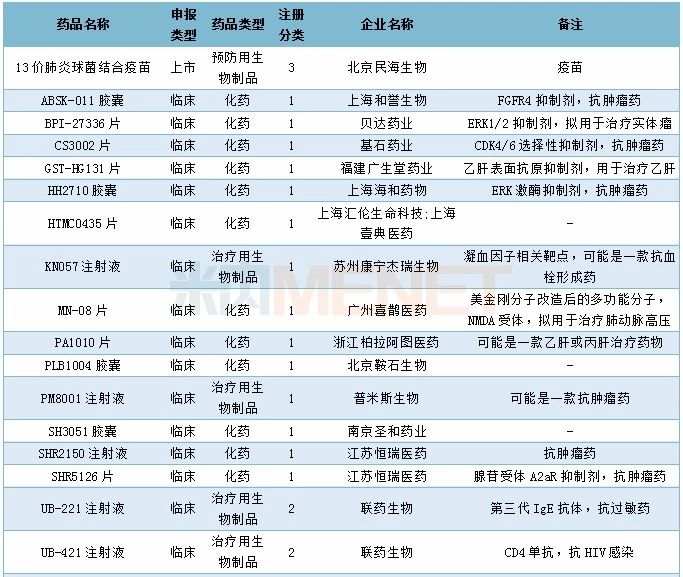
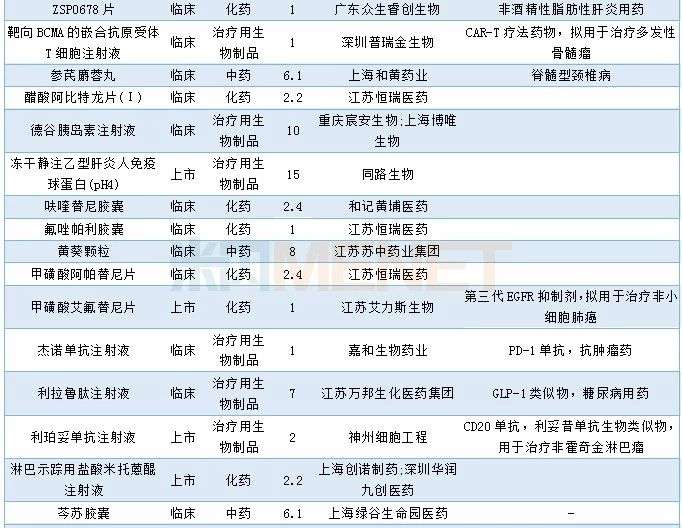
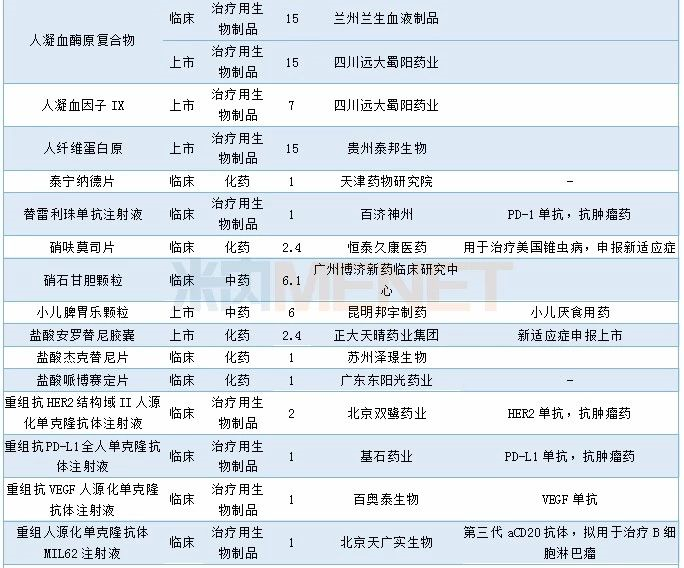
2019年12月国内新药申请承办情况

仿制申请承办情况
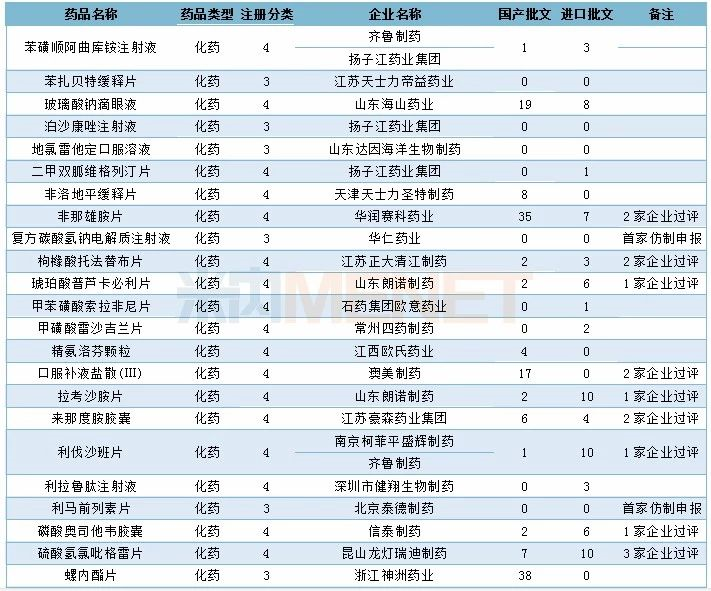
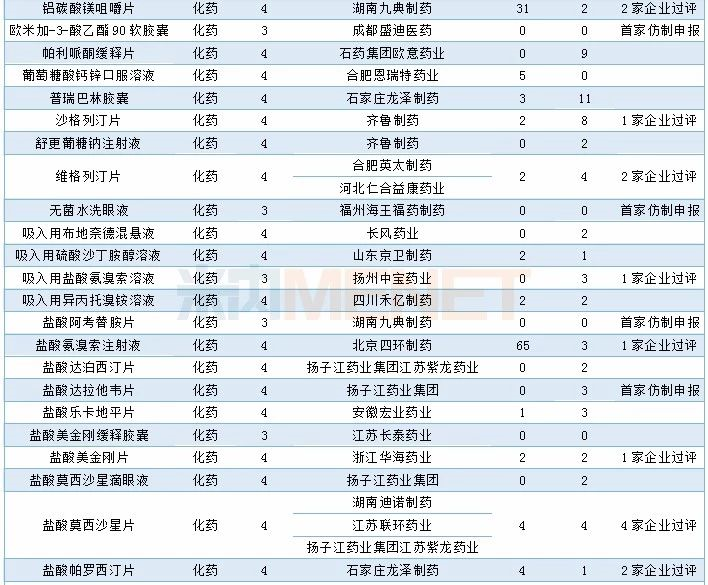
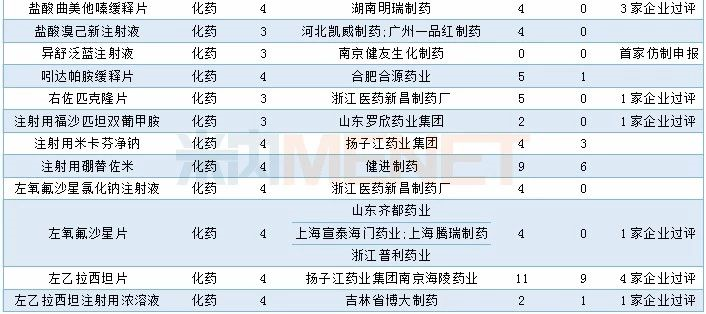
12月CDE共承办58个品种的仿制申请,其中按3类仿制申请的品种有15个,按4类仿制申请的品种有43个,23个品种目前已有企业通过一致性评价,7个品种有首家企业提交仿制申报。详细情况请见下表:
2019年12月国产仿制申请承办情况
进口申请承办情况
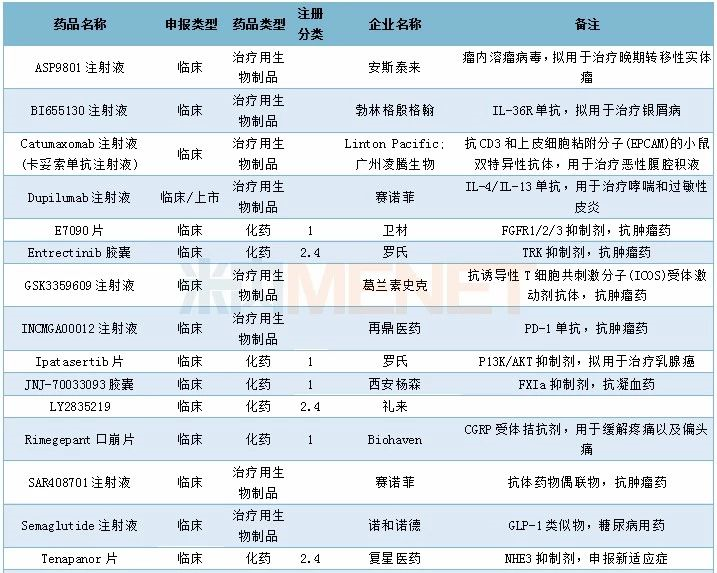
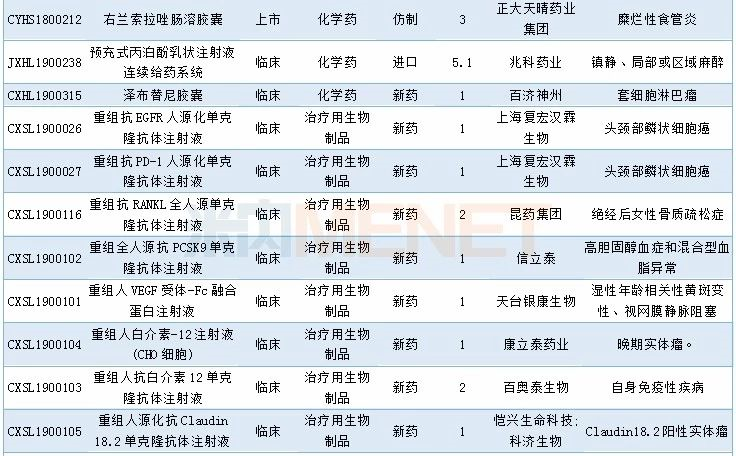
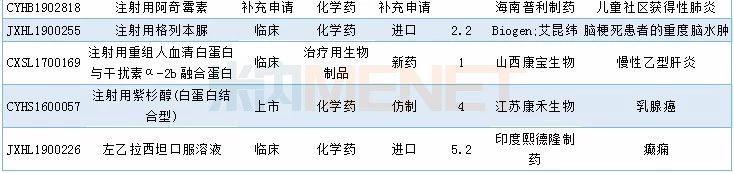
12月CDE共承办40个药物的进口申请,其中1类新药有5个,2.4类改良型新药有5个,5.1类进口原研药8个,5.2类进口仿制药6个。具体情况请见下表:
2019年12月进口申请承办情况
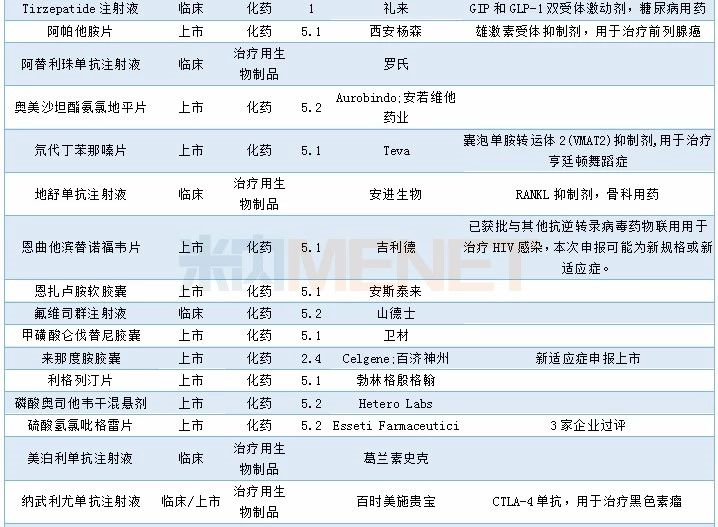
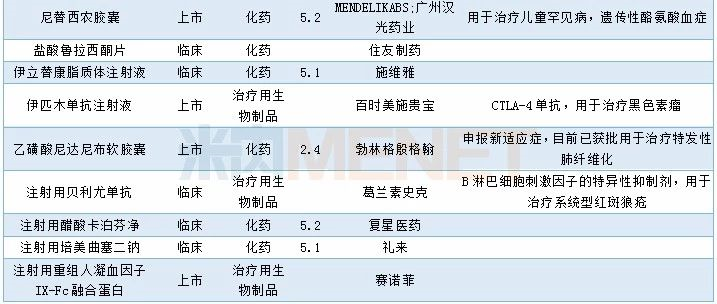
审批情况
12月有多个新药获批,其中1类新药4个,6.1类中药新药1个。此外还有3个3类仿制药、16个4类仿制药获批。20个品种有企业通过一致性评价,其中盐酸二甲双胍片有4个企业过评。91个品种(涉及149个受理号)获临床试验默示许可。具体情况请见下表:
2019年12月部分品种获批情况
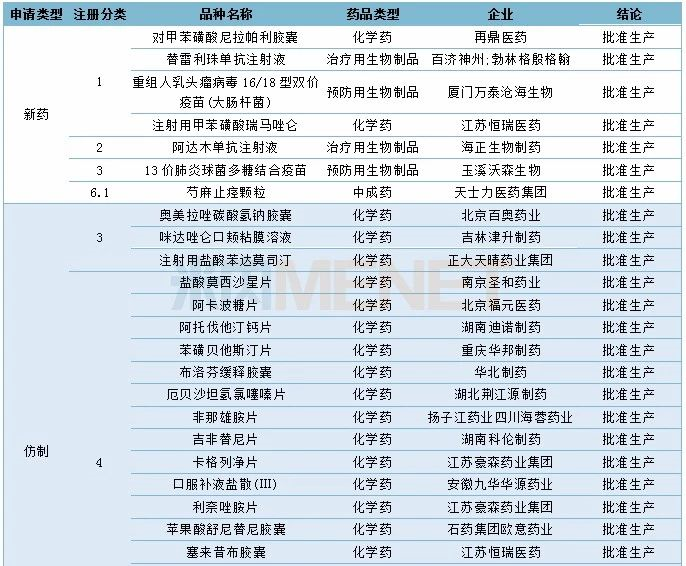
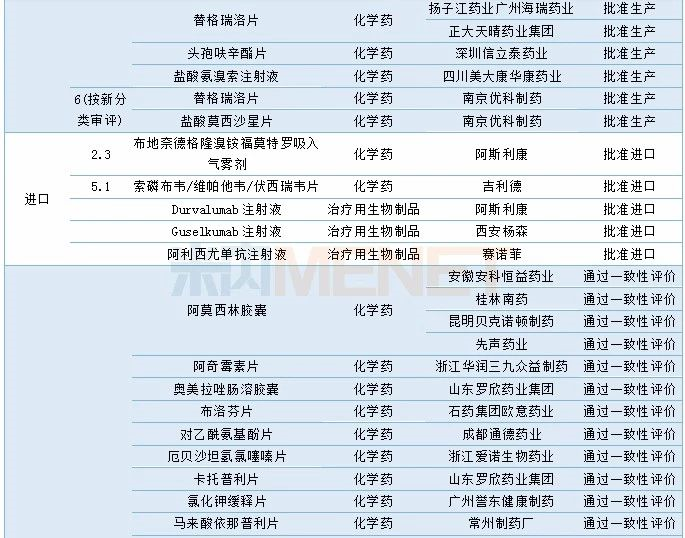
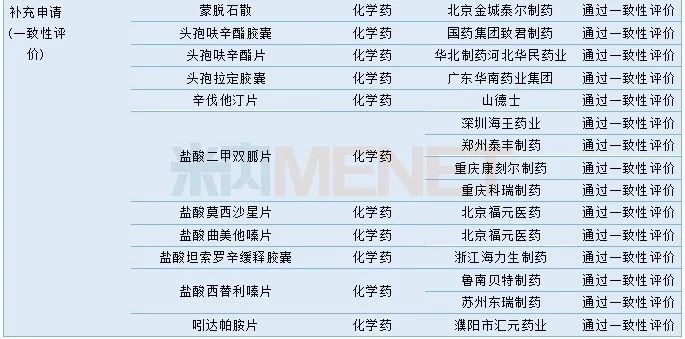
(说明:按企业公告或相关报道统计获批时间)
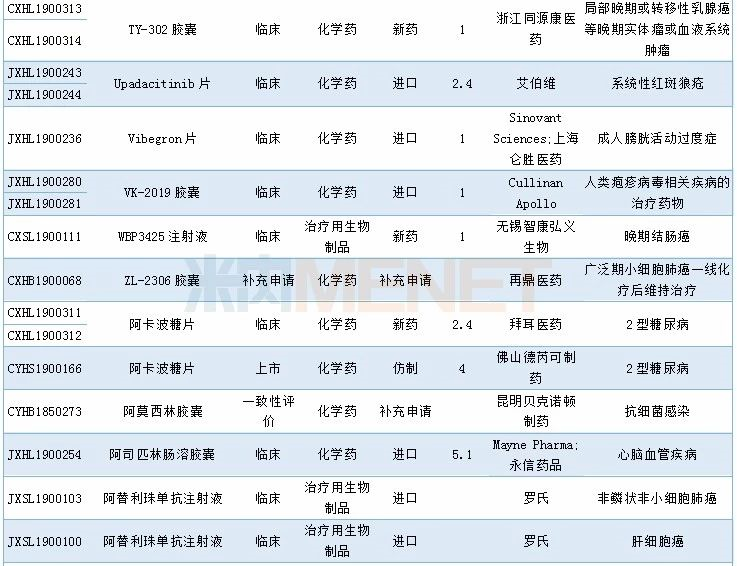
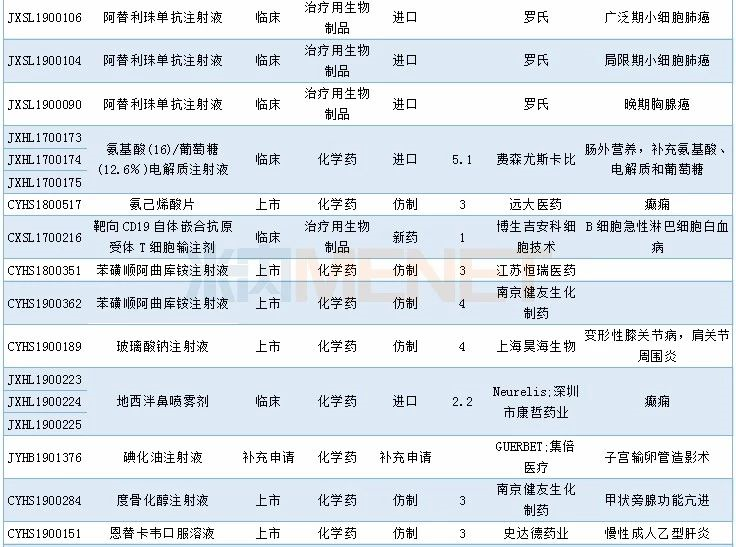
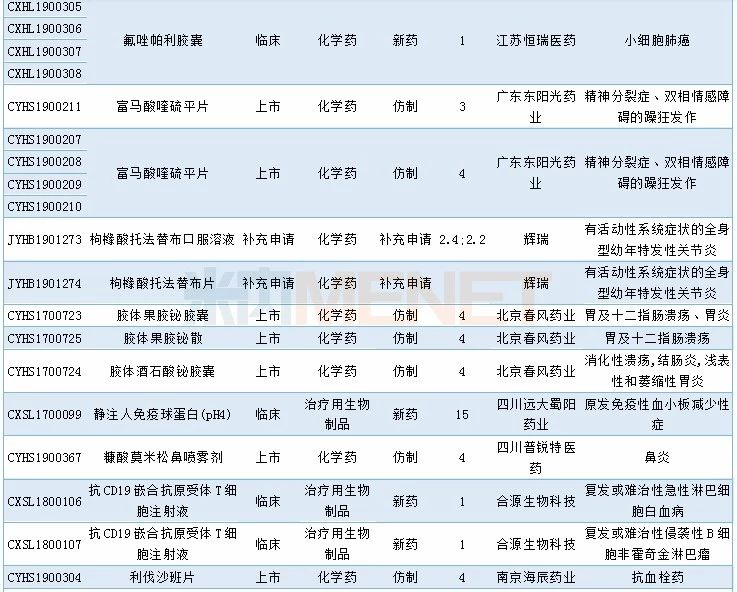
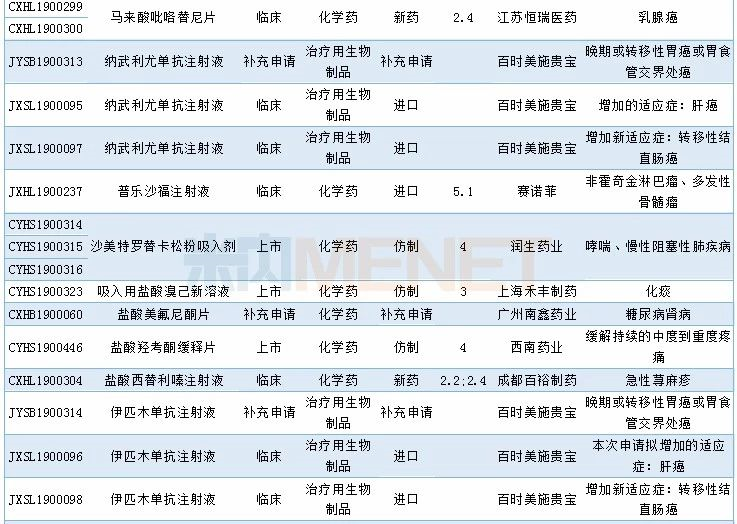
2019年12月临床试验默示许可药品
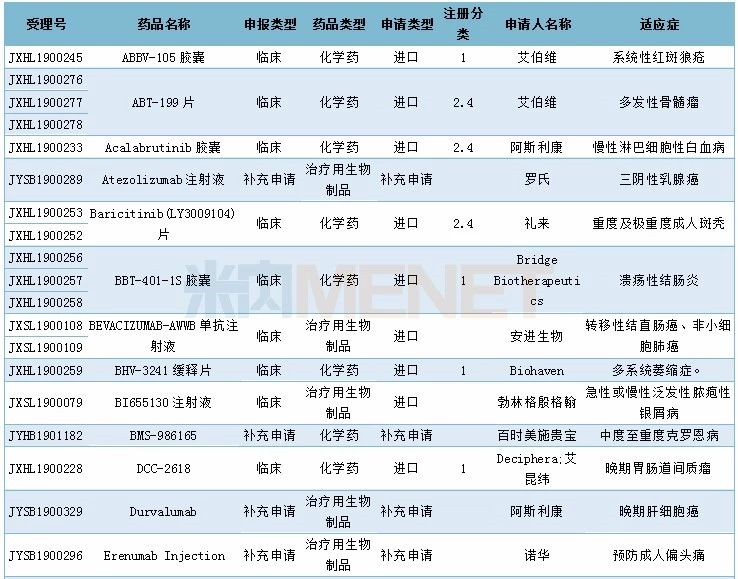
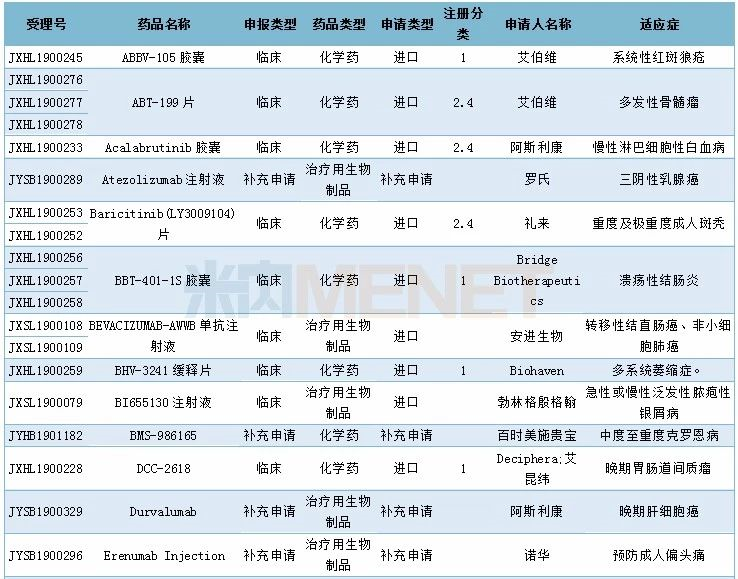
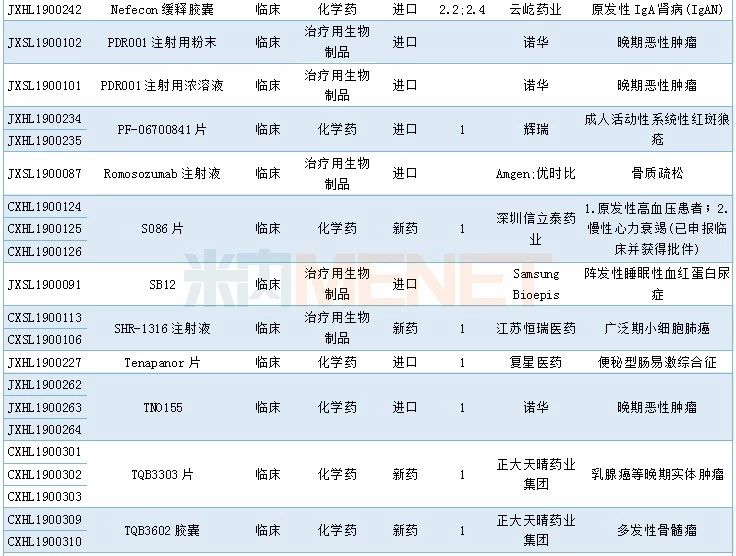
如果这篇文章侵犯了您的权利,请联系我们。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx