来源:博悦汇 作者:东哥
参比制剂信息
1、国内上市情况
目前国内二甲双胍肠溶片(胶囊)有20个文号,有0.25g和0.5g两种规格。
无进口药品。
无进口本地化产品上市。
2、国外上市情况
未查到国外有肠溶制剂上市
3、参比制剂
未查询到国外有盐酸二甲双胍肠溶制剂上市,只在中国上市,无法确定参比制剂。
小编点评:
二甲双胍肠溶制剂只在国内上市,无参比制剂可选,这种情况一致性评价过程中需要进行验证性临床试验了。另外FDA目前已上市肠溶制剂(不是二甲双胍)有拿普通制剂做参比进行BE试验的先例,可以考虑用施贵宝的格华止做参比进行BE研究,当然首先要分析格华止的体内药时曲线并结合预实验情况判断是否可行。
原料药性质
解离常数:pKa = 12.4(针对仲氨基)
在各溶出介质中的溶解度(37℃):
pH1.2:333mg/ml
pH4.0:353mg/ml
pH6.8:355mg/ml
水:346mg/ml
在各溶出介质中的稳定性:
水:未测定。
在各pH值溶出介质中:未测定。
光:未测定。
BCS分类:Ⅲ类
小编点评:
对于高溶解性(BCS 3类)药物,采用常规辅料和生产技术制备的普通口服固体制剂,建立体内外相关性较为困难。
制剂处方
未查到二甲双胍肠溶制剂的处方,可参考格华止的片剂处方。
小编点评:肠溶制剂中辅料可参考片剂中的辅料,根据溶出和BE情况调整处方和工艺。
溶出曲线(pMDA)
溶出曲线(日本普通片剂)
PMDA溶出方法:桨板法,水900ml为溶出介质,转速为50rpm,经120分钟(A型)或15分钟(B型)取样,限度为标示量的85%(A型)或80%(B型)
溶出度试验条件:桨板法/50转、溶出介质中不添加表面活性剂。
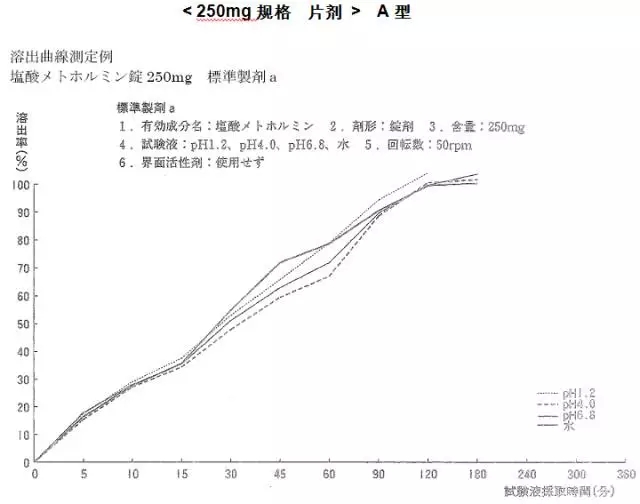
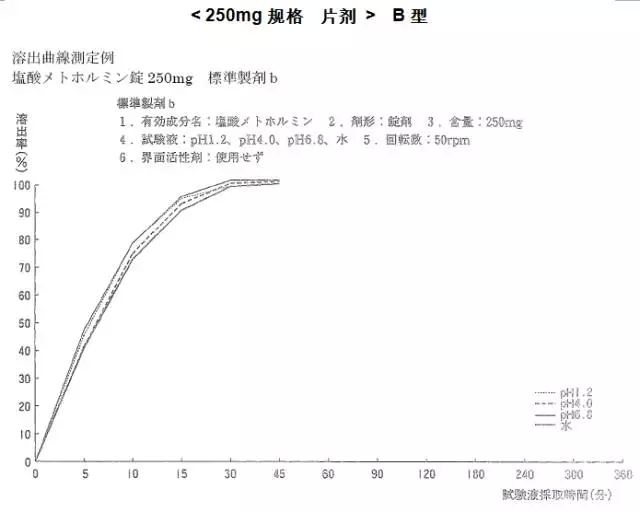
小编点评:
日本的溶出曲线仅供参考,肠溶制剂很难与普通制剂比较溶出曲线,最终还需要通过临床来验证产品的有效性。
有关物质
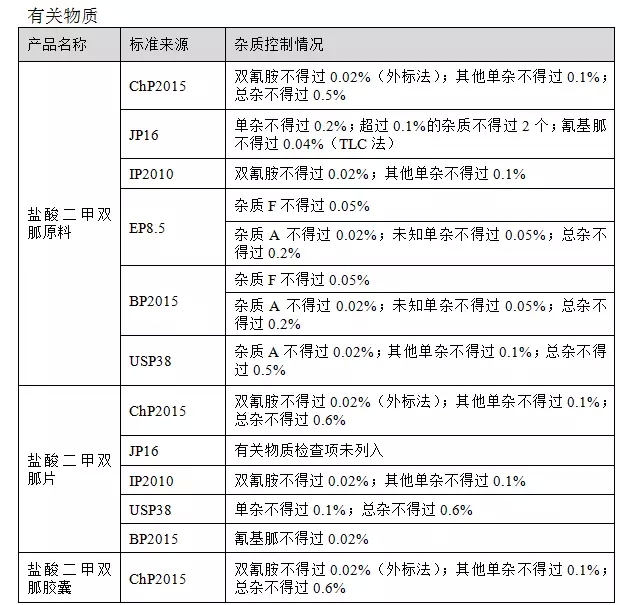
小编点评:
国外药典无盐酸二甲双胍肠溶制剂标准收载,可参考片剂或其他口服剂型进行有关物质研究。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx