屋漏偏逢连夜雨,就在前不久三生制药终止与阿斯利康的许可协议,放弃GLP-1百泌达在中国区的商业化工作之后,如今在研管线也遭遇新变化。
据媒体报道,阿斯利康日前决定终止开发GLP-1R/GCGR双重激动剂Cotadutide的部分临床试验,并将研发资源向新的GLP-1R/GCGR激动剂AZD9550倾斜。

就在阿斯利康决定调整GLP-1产品研发策略之际,4月13日,诺和诺德宣布上调2023年营收和利润的增长预期,预计2023年营收增长24-30%。不难感受到,GLP-1药物火爆席卷全球,诺和诺德似乎先人一步拿到了“船票”。
另一方面,礼来紧随其后,不仅此前Tirzepatide产品在SURPASS-2研究“头对头”击败司美格鲁肽,引发行业轰动;并且,在今年4月,礼来发布消息称,口服小分子 GLP-1R 激动剂 Orforglipron将开展一项III期临床试验(ACHIEVE-4)。
此消彼长之间,诺和诺德与礼来的两强相争,也让越来越多的人关注这一领域。业内人士表示,在诺和诺德攻城略地、礼来强势追击的局面下,一款GLP-1领域产品如果没有特别突出的临床优势,很难在激烈的市场竞争中分得蛋糕。阿斯利康取舍之间,也给GLP-1细分赛道的参与者带来了一些启示。
阿斯利康调整管线
新产品或另辟蹊径
近年来,GLP-1R、GIPR、GCGR等靶点的双重激动剂,临床价值逐渐得到关注,多靶点GLP-1药物成为行业热点。虽然艾塞那肽逐渐退出市场,但阿斯利康一直以来都是GLP-1赛道上的重要参与者,并且积极跟进了双激动剂的研发。
Cotadutide是MedImmune(于2007年被阿斯利康收购)研发的一款GLP-1R/GCGR双重激动剂,然而,这款产品的临床开发道路并非一帆风顺。
临床前研究显示,cotadutide的小鼠体内血浆半衰期约为5h,与利拉鲁肽相近(约7h);在头对头利拉鲁肽的IIb期研究(N=834)中,cotadutide所有剂量组的减重和降糖效果均不亚于利拉鲁肽组。
据阿斯利康在2021年公布的IIb期临床结果显示,与利拉鲁肽相比,Cotadutide并没有能够在降糖和减重方面显示出巨大的临床优势,市场对此不无失望。
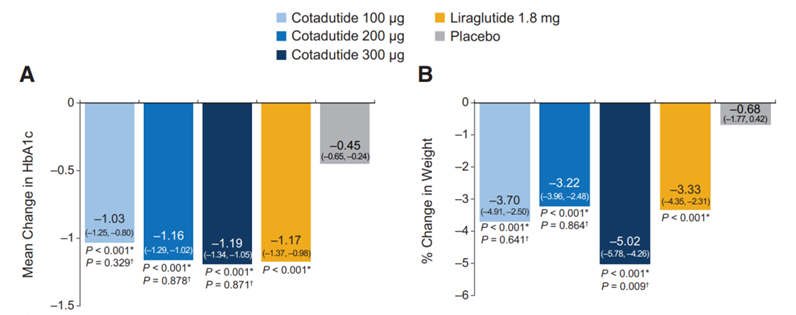
随后,在阿斯利康研发管线信息披露中,Cotadutide治疗2型糖尿病、肥胖症以及糖尿病肾病等3个适应症的开发被剔除Ⅱ期临床管线。
而据本次最新消息,阿斯利康进一步终止了Cotadutide在3个领域的临床试验:非酒精性脂肪肝炎(NASH)、肝损伤、心脏复极化。对此,阿斯利康方面表示,目前正在结束Cotadutide临床试验的患者招募,而已入组的患者有权选择是否继续接受治疗。
截至目前,Cotadutide已完成4项II期研究。在一项针对伴2型糖尿病的超重或肥胖患者的IIa期研究(N=113)中,cotadutide组体重显著减轻(-3.84kg vs -1.70kg;P=0.0008),HbA1c水平亦显著下降(-0.9% vs -0.6%;P=0.0004)。
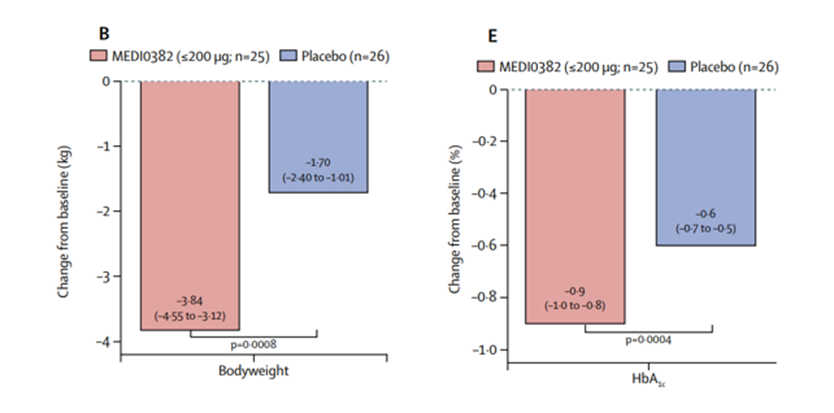
市场人士对此不无惋惜,有观点认为,在竞争一直处于白热化的糖尿病赛道上,横空出世的GLP-1迅速在疗效上压过该领域原有霸主胰岛素一头;除此之外,GLP-1还拓展了肥胖/超重领域,在更广阔的领域展现强大的能力。“虽然GLP-1领域的市场竞争愈发转向更长的半衰期、更持久的药物作用时间、更少的用药次数,但也不是所有患者都耐受和适用长效制剂,短效产品依然存在一定的市场空间。”
事实上,短效制剂的市场依然存在,据诺和诺德公司2022年年报显示,利拉鲁肽2022年全球销售额为123.22亿丹麦克朗(约为人民币123.28亿元)。
然而,即便如此,对于做出放弃Cotadutide研发决定的阿斯利康而言,尽管在临床试验的推进中耗费了大量人力物力,但是如果继续投入,后期上市的商业化费用与时间成本将可能给阿斯利康带来更多的沉没成本。
此时壮士断腕,也可以将有限的精力和资金放在其他机会更大的产品上。毕竟,阿斯利康终止开发Cotadutide,并不意味着放弃了这条黄金赛道,其在GLP-1领域的布局并非只有该药。在报道中,阿斯利康表示将集中资源开发一款同机制药物 AZD9550,与cotadutide每日一次给药不同的是,该药是周制剂;除此之外,阿斯利康管线中还有一款口服GLP-1R激动剂AZD0186正在开发中。
诺和诺德、礼来两强相争
GLP-1竞争大戏连台
MNC宣布优化管线,如今并非新鲜事,尽管可能会面临较为艰辛的商业化局面,但骰子没落地之前,谁也不知道结果。此时阿斯利康的在后期产品有望迎来商业化之际做出调整,无疑给行业传递了不同的信号。
如今的GLP-1赛道,诺和诺德与礼来已经呈现两强相争的局面。4月13日,诺和诺德宣布上调2023年营收和利润的增长预期。

由于司美格鲁肽在第一季度的收入增长大大超过了之前的预期,诺和诺德预计按固定汇率计算的全年营收将增长24%至30%,此前为13%至19%;全年经营利润将增长28%至34%,此前为13%至19%。受此消息影响,截至本周收盘,诺和诺德股价大涨。以167.61美元/股,2.5%增幅再创历史纪录,市值达到3770亿美元。
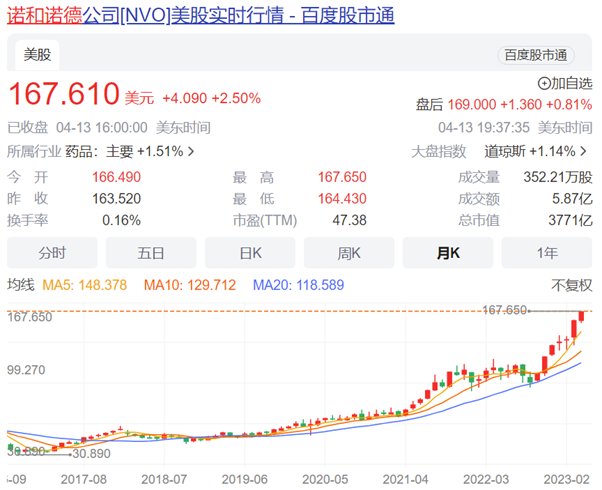
前不久,诺和诺德的口服司美格鲁肽还在国内启动一项III期临床试验,将肥胖适应证拓展至中国,这也是口服司美格鲁肽在国内启动的第一项针对减肥适应证的III期临床研究。该消息一出,为诺和诺德再添一把火。
另一方面,礼来于今年2月宣布,其在研的减肥药物GIP和GLP-1双受体激动剂Tirzepatide(替尔泊肽)用于肥胖或超重成人患者的中国III期临床试验,取得积极结果,达到主要终点和所有关键次要终点。此前(2021年3月),礼来还公布了该药与诺和诺德的司美格鲁肽头对头临床试验的积极结果。
在4月,礼来又发布消息称,在clinicaltrials.gov网站上登记了一项III期临床试验(ACHIEVE-4),旨在评估口服小分子 GLP-1R 激动剂 Orforglipron(递增剂量,每日1次)对比甘精胰岛素(个性化剂量,每日1次)在心血管风险增加的成人2型糖尿病患者和成人肥胖或超重患者中的安全性和有效性。这项大型临床试验目标覆盖超过2600名糖尿病或超重受试者,使 Orforglipron 成为同类药物中首个步入临床III期阶段的产品。
在诺和诺德、礼来的你追我赶中,GLP-1潜力正在不断显露和释放。如今,GLP-1称霸糖尿病市场已经没有争议,并不断开拓减重、NASH、CKD、AD等新的适应证,每一个都将是超级大市场。
业内专家表示,在GLP-1赛道,除了有诺和诺德、礼来这样的巨头,安进、辉瑞、信达生物等玩家同样来势汹汹,阿斯利康选择押注机会更大的AZD9550和AZD0186,显然有着更多思考,同时也预示了,双靶点、多靶点、周制剂、口服制剂,市场竞争的“门槛”正在大幅抬升。
国内也有不少企业看到了机会,信达与礼来合作的IBI362 领跑,华东医药、众生药业、正大天晴等也积极加入该领域的赛跑,谁能上演me-too、me-better尚有待进一步观察。
值得关注的是,3月30日,华东医药发布公告,全资子公司杭州中美华东收到国家药监局核准签发的《药品注册证书》,由中美华东申报的利拉鲁肽注射液(商品名:利鲁平)上市许可申请获批,用于成人2型糖尿病患者控制血糖。国内“首仿”切入赛道,亦将掀起市场波澜。

行业普遍认为,曾经靠同类竞争,选择更优的模式已经被淘汰,GLP-1与DS-8201就是最好的例子。未来谁能有更长远的目标与更完善的研发体系,谁能利用好前沿技术并在“真创新”的道路上坚定不移的走下去,谁才能在竞争中脱颖而出。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx