今日,A股医药板块迎来了久违的爆发式大涨。
值得关注的是,首药控股20CM涨停,泽璟制药、海创药业、百济神州、迪哲医药、艾力斯、亚虹医药、贝达药业、荣昌生物等涨超10%,奥赛康、海思科涨停,尤其是带“U”字标识个股,即科创板上市时发行人尚未盈利的企业,更是受到了投资人的热捧。
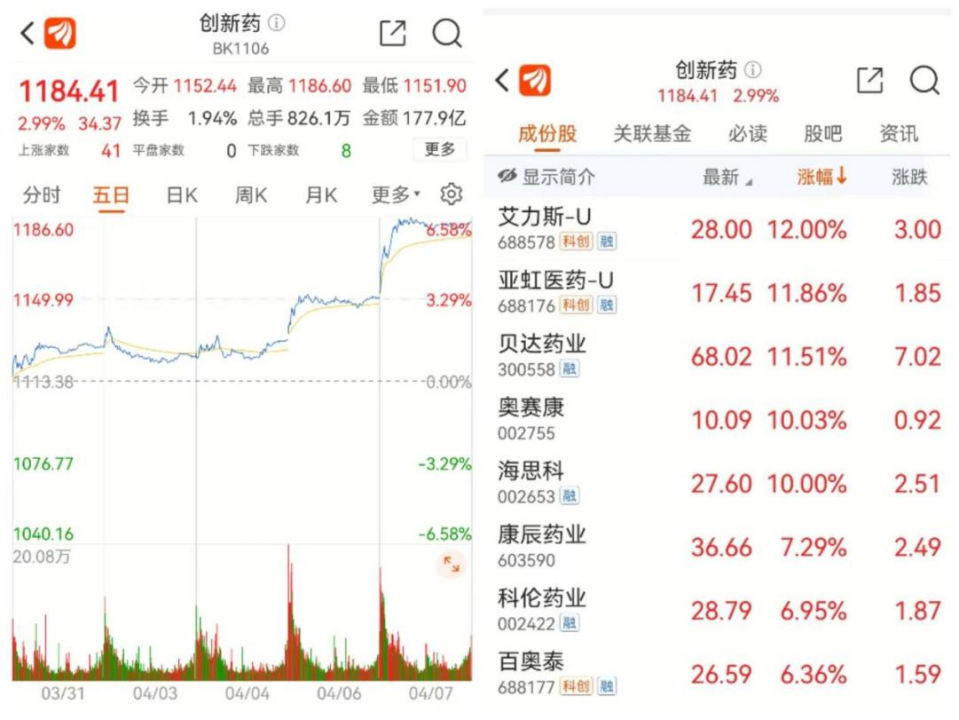
行业普遍认为,本次资本市场对“医药创新”概念的热捧,与日前国家药品监督管理局药品审评中心(CDE)发布《药审中心加快创新药上市许可申请审评工作规范(试行)》(下称《规范》,原文见文末)有关。《规范》旨在鼓励研究与创制新药、满足临床用药需求,加快创新药品的审评审批。
政策改革创新利好持续释放,同时国内A股上市药企2022年年报陆续发布,“创新升级”主题成为了企业转型的核心战略。包括上海医药、先声药业等在内的一大批大型制药企业,在创新药研发方面下足力气,纷纷展示亮眼成绩。
市场观点指出,经历了过去两年的资本“寒冬”,如今政策利好和营收大涨的双重因素叠加,二级市场对医药创新的信心正在开始恢复。整体医药板块反弹上扬,预示着国内医药产业正在迎来新药研发、上市的新一轮爆发期,产业链在经历洗牌之后也将呈现出崭新态势。
《规范》是继《药品注册管理办法》、《突破性治疗药物审评工作程序(试行)》等一系列鼓励创新药品政策的落地细则后的深入推进和继续探索。
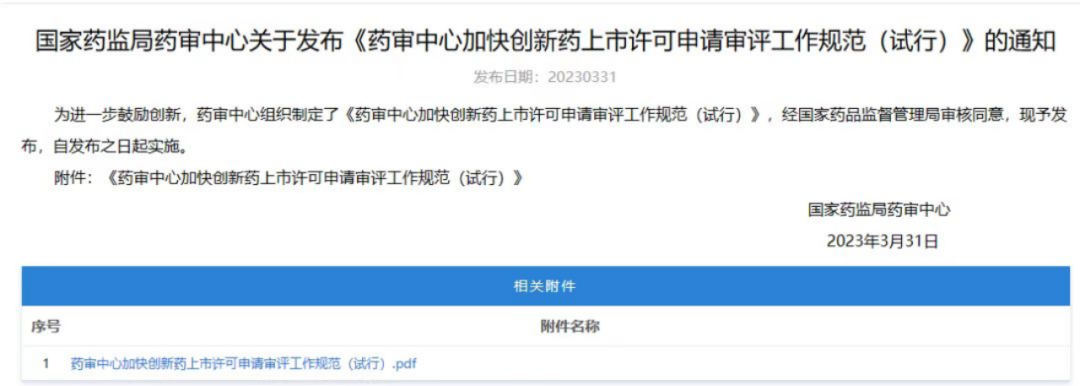
此前(2020年7月),药审中心发布《突破性治疗药物审评工作程序(试行)》,适用于药物临床试验期间,用于防治严重危及生命或者严重影响生存质量的疾病且尚无有效防治手段或者与现有治疗手段相比有足够证据表明具有明显临床优势的创新药或者改良型新药等。
2022年2月,CED曾发布《药审中心加快创新药上市申请审评工作程序(试行)》(征求意见稿)。本次《规范》发布后,无疑新药上市的具体要求与操作办法落地,行业翘首以盼的重大利好终于出台。
1. 适用范围:儿童专用创新药、用于治疗罕见病的创新药以及纳入突破性治疗药物程序的创新药,特别审评审批品种除外;
2. 使用研发阶段:探索性临床试验完成后,已具备开展确证性临床试验条件至批准上市前;
3. 时限要求:沟通交流时限为30日,品种审评时限同优先审评品种时限为130日,按照单独序列管理。
制定该工作程序的初衷是为了鼓励研究和创制新药,满足临床用药需求,加快创新药品的审评速度。在业内看来,该工作程序以制度形式转化、巩固和扩大我国之前在新药研发领域的探索成果与宝贵经验,将更加有力地帮助申请人推进药物的临床研发,加快相关创新药物的上市步伐。
在审评过程中,CDE将通过早期介入、研审联动、滚动提交等方式,将在整个临床和上市申报阶段,缩短儿童用药、罕见病用药以及创新药品的研发进程,加快创新药品种审评审批速度,节省研发开支。
值得注意的是,对于行业来说受到影响的企业远不至于创新药企,涉及相关产业的细分赛道也将迎来一波发展期。如创新药产业链的CXO、上游供应商,高壁垒制剂以及原料企业,甚至医疗器械行业也将得到助益。
近年来,在政策支持下,我国新药审评审批不断提速,创新药正加速落地,多年来屡创新高。2021年,NMPA共批准32款创新药(化药和治疗用生物制品)上市,2022年批准超40款,屡创新高。
新药研发是一个高风险、高投入的长期探索过程。本次《规范》充分考虑了新药研发的实际需求,业界普遍认为,随着《规范》公布与明确,突破性治疗药物有望进一步缩短其上市进程。
不过有业内专家提醒,突破性治疗药物认定为相关药企在药物研发带来的首要价值是与监管机构更多的沟通交流机会,并非获批上市的承诺,药企需要认真把握这一寻求技术支持的绝佳途径。
而随着科学技术和药物研发的不断进展,未来突破性治疗药物认定的标准门槛势必将越来越高,药物的临床价值永远是监管机构考虑的第一要素,产品只有取得临床疗效上的真正突破,方有资格角逐突破性治疗药物的这一黄金赛道。期待未来我国新药研发再攀高峰。
近年来,随着我国药品审评审批制度改革加速深化推进,鼓励药品创新政策红利不断加码,审评能力与效率进一步提升,审评资源重点投向重大创新、临床急需、临床价值突出、公共卫生急需的药物,极大地激发了全行业药品创新潜能,国内各大药业也纷纷在近期展示多方助力下的新药成果。
3月末,先声药业发布2022年度业绩公告。报告期内,先声药业共实现总收入63.19亿元、较去年同期增长26.4%。引人注意的是,公告指出,2022年先声药业创新药业务收入约41.28亿元,占总收入的65.3%,较2021年31.20亿元增长约32.3%。
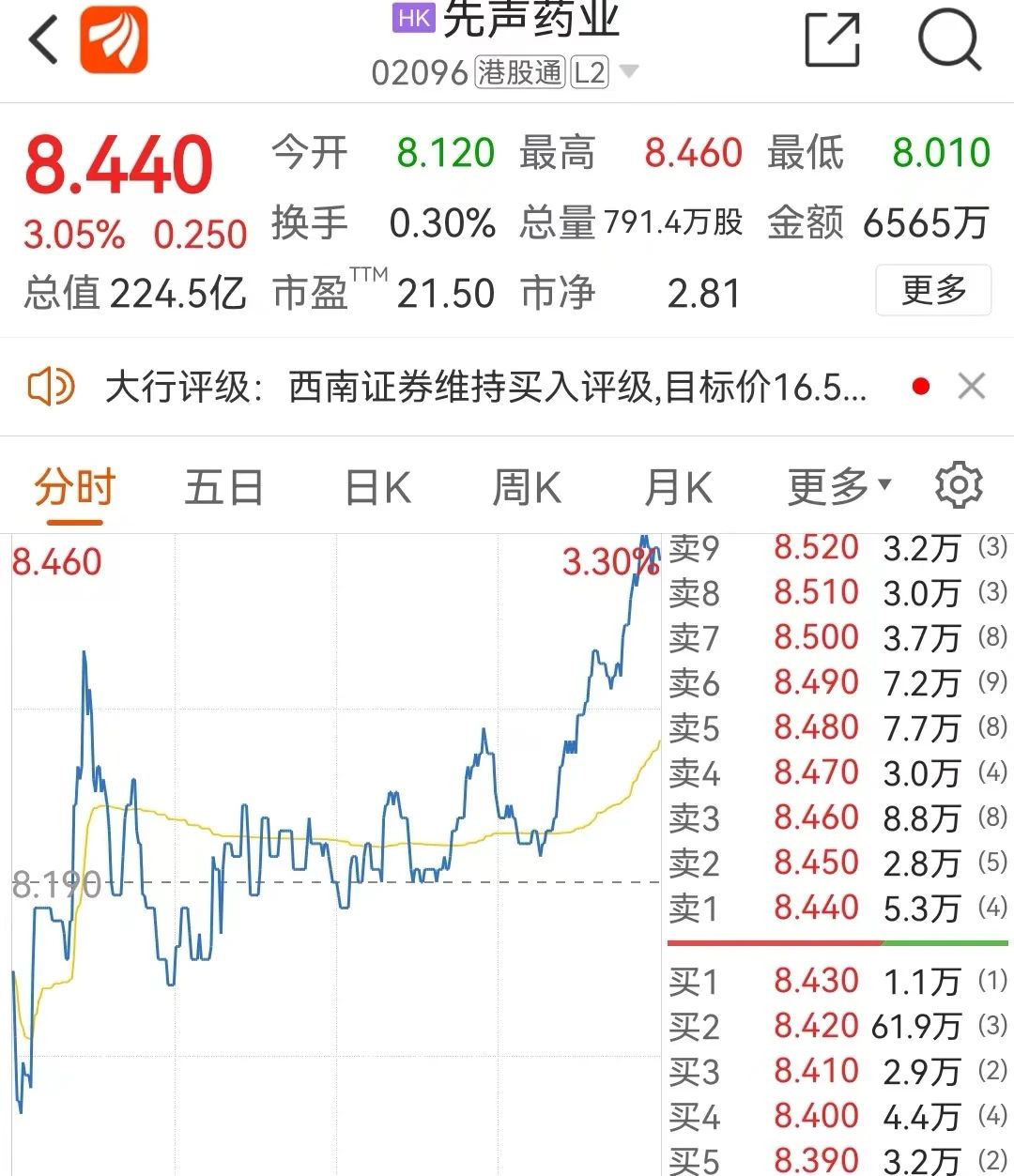
据了解,先声药业此次成绩是基于新获批上市的2款创新药产品,至此,先声药业目前已进入商业化阶段的创新药扩充至6款。不仅如此,先声药业在创新研发上的投入更多,未来将有机会带来更多创新药。公告显示,先声药业目前其拥有创新药研发管线近60项,现正就17种创新药开展注册性临床研究。
无独有偶,上海医药也发布了最新年报。上海医药表示,科技创新步入收获期,稳重求进培育新增长。2022年,上海医药实现营业收入2319.81亿元,同比增长7.49%。同时,研发投入高达28.00亿元,同比增长11.87%。截至2022年末,该公司已有安柯瑞(重组人5型腺病毒)、凯力康(尤瑞克林)、培菲康(双歧杆菌三联活菌)3款1类新药上市,临床申请获得受理及进入后续临床研究阶段的新药管线已有62项,其中创新药50项,改良型新药12项。

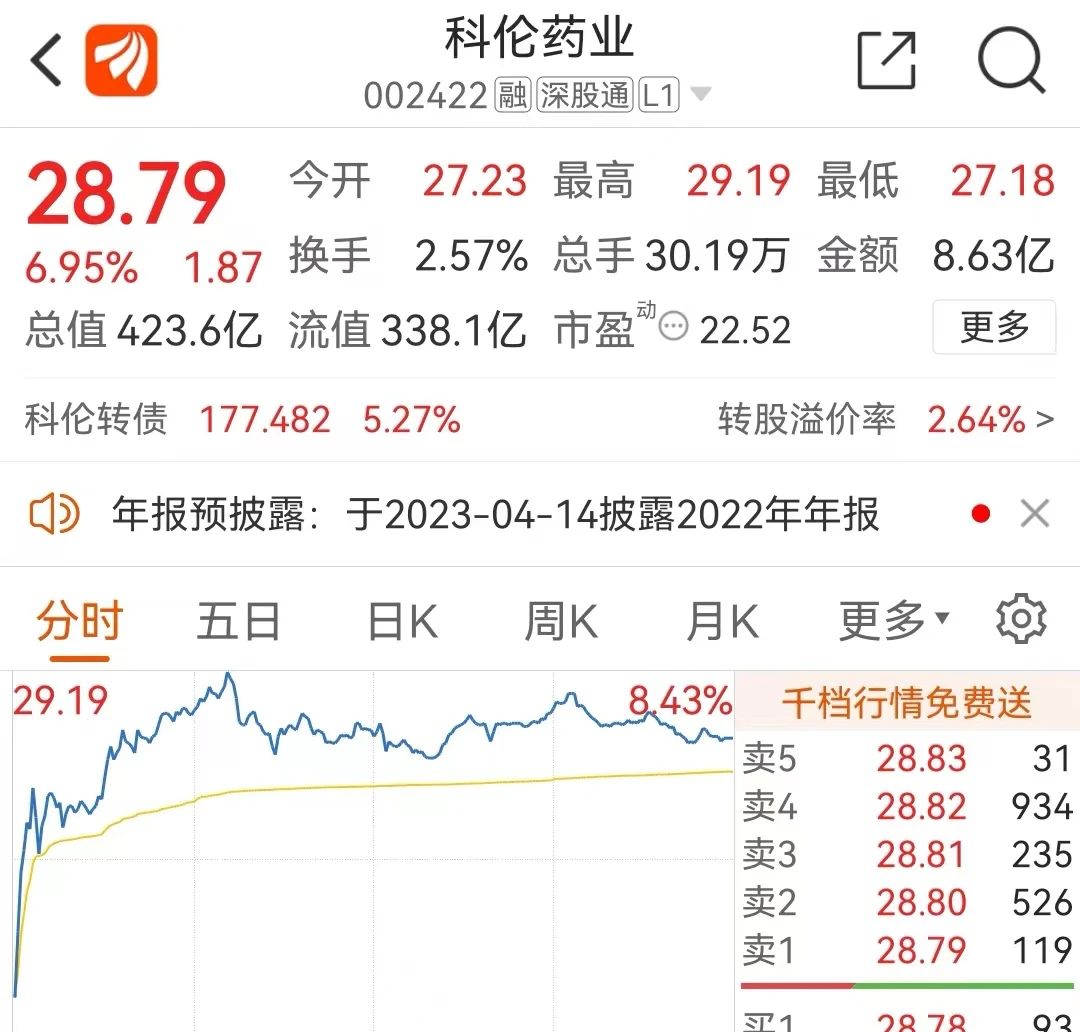
股市大涨的还有科伦药业,在此前公布的业绩预告中,其2022年度业绩预预计净利润预计16-17亿元,同增45%-56%,主要之一系创新研发项目。据了解,科伦药业ADC+MSD催化剂丰富,2022年其项目A、项目B、7个ADC授权给MSD,协议金额为14、9、95亿美元。
另外,聚焦泌尿生殖系统疾病的全球化创新药企亚虹医药也成为本次补涨受益者。该企业目前临床管线包括9个产品、12个在研项目,主要布局泌尿系统和生殖系统疾病,其中核心产品APL-1202和APL-1702已进入III期临床。
业内人士指出,当下“红火”局面是多方互利、共同作用的结果。创新药研发上市数量不断创新高,尤其是突破性治疗药物不断涌现,是政策倾斜的结果,也是企业在不断提高的研发能力与生产技术作用下,营收持续增长,反哺行业的必然。我国患者也因此更快地用上了新药、好药。
回顾此前行业动向,半个月内,也有多家公司透露自家新药研发的积极进展。随着创新药研制再度迎来政策鼓励支持,新药即将迎来集中获批期。
首药控股3月17日公告称,收到关于第三代ALK激酶抑制剂SY-3505沟通交流申请附条件批准上市资格的反馈意见,同意SY-3505开展拟定单臂设计研究。公司将迅速启动SY-3505针对二代ALK抑制剂耐药的非小细胞肺癌患者的关键性Ⅱ期临床试验。
贝达药业3月30日在投资者互动平台表示,公司正努力推进恩沙替尼境外申报上市的工作,贝福替尼术后辅助III期临床研究也已经完成首例受试者入组。
艾力斯4月4日公告,伏美替尼针对EGFR或HER2突变晚期NSCLC患者的Ib期临床试验获得药物临床试验批准,伏美替尼20外显子插入突变NSCLC一线治疗适应症获得药物临床试验批准。
海思科4月5日公告,其全球首家口服AR-V7降解剂,HSK38008口服制剂于近日获得CDE下发的《药物临床试验批准通知书》,同意本品开展用于治疗“前列腺癌”的临床试验。
……
事实上,产业发展转型升级的主旋律并没有发生改变,创新仍是医药行业持续发展的本源,符合产业进化趋势的细分赛道及对应公司有更大机会能够穿越周期,实现可持续的发展。
行业专家分析指出,医药创新顶层政策推动,医保支付端对创新药的支付力度也在持续加大,“唯低价是取”不再是支付端衡量药品价值的唯一准绳;部分企业加速推出的创新产品将有望为公司带来重要催化剂,不仅为公司业绩赋能,还将带动行业正向循环发展。2023年市场将有望进一步回暖,医药行业投融资活跃度不断回升,行业发展将从方方面面被注入信心。

【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx