2 月 24 日,亿帆医药宣布,子公司亿一生物的长效升白药「艾贝格司亭 α 注射液」(拟用商品名:亿立舒)上市申请已经正式获得 CDE 受理,用于预防及治疗肿瘤患者在化疗过程中引起的嗜中性粒细胞减少症。

来自:亿帆医药公告
在 2021 年 8 月 26 日,亿一生物已经与正大天晴就 F-627 达成了合作,以 3000 万元首付款 + 最高可达 1.8 亿元里程碑款 + 分级净销售额提成费将 F-627 在中国境内的所有知识产权和商业化权益独家许可给天晴南京顺欣,交易总额超过 2.1 亿元。天晴南京顺欣受让 F-627 药品上市许可后,将委托北京亿一进行生产。
历时十一年研发,2021 年已在欧美申报上市
艾贝格司亭 α 注射液(曾用名:重组人粒细胞集落刺激因子-Fc 融合蛋白,研发代号:F-627)是基于亿一生物现有具有自主知识产权 Di-KineTM 双分子技术平台开发的创新生物药品种,是基于 Fc 融合蛋白技术,由 CHO 细胞表达的 rhG-CSF 二聚体,具有长效和强效的生物学特点。目前,F-627 主要应用于预防及治疗肿瘤患者在化疗过程中引起的嗜中性粒细胞减少症,可使肿瘤化疗患者嗜中性粒细胞迅速增殖和恢复,从而增强了免疫系统抵抗感染的能力,以防止患者在化疗期间死于感染或者其他相关并发症。
根据 Insight 数据库,F-627 项目早在 2010 年就启动临床研发,在国内首项临床申请在 2011 年初就已经提交。目前在国内,F-627 共启动了 6 项临床,包括 1 项 III 期临床(点此查看:CTR20170705)。
贝格司亭国内项目详情 点此查询
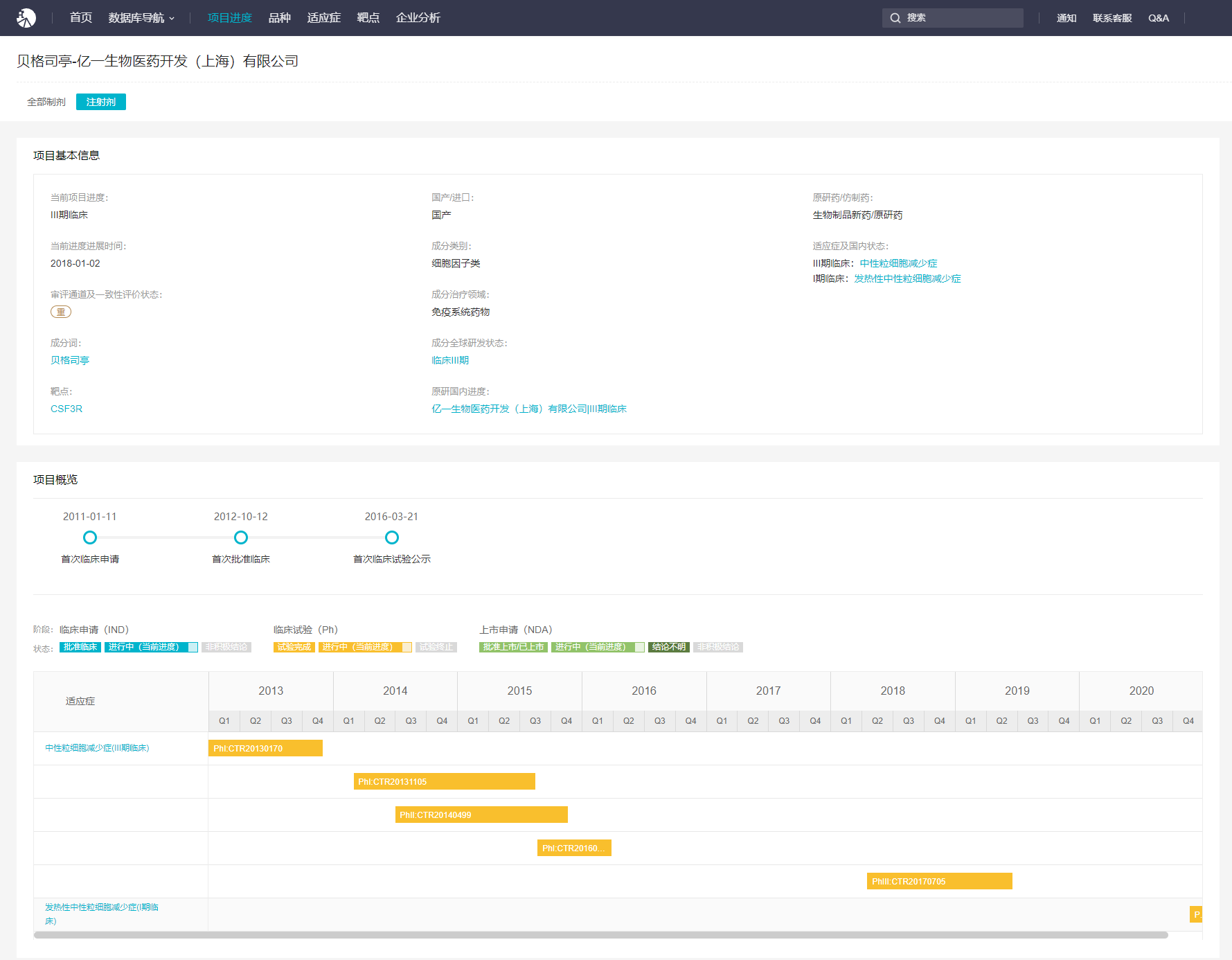
来自:Insight 数据库(http://db.dxy.cn/v5/home/)
全球上市方面,F-627 在 2021 年就已经先后在美国、欧盟申报上市。全球首项临床早在 2010 年就在澳大利亚启动,至申报上市时已经经历了 11 年的临床研发。
F-627 项目全球开发关键节点
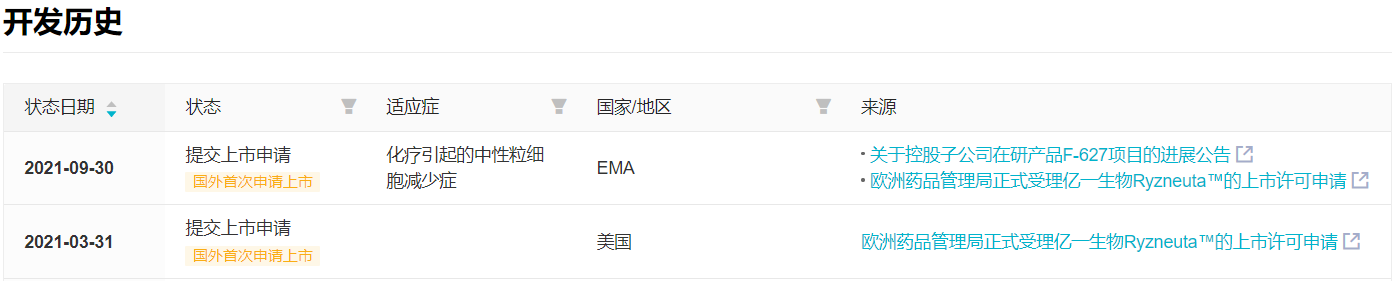

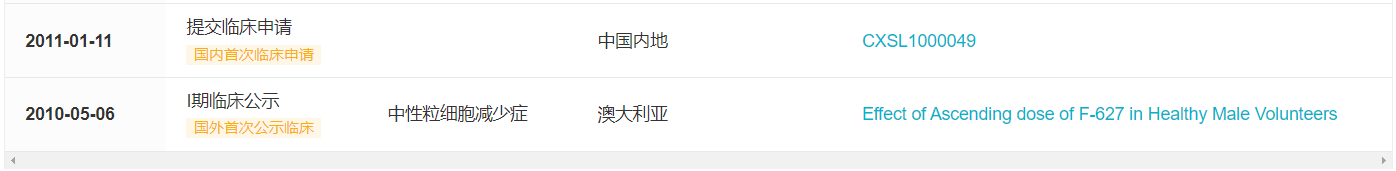 来自 Insight 数据库全球新药模块(http://db.dxy.cn/v5/home/)*截图仅展示关键节点,项目全开发历史可至 Insight 数据库内查看
来自 Insight 数据库全球新药模块(http://db.dxy.cn/v5/home/)*截图仅展示关键节点,项目全开发历史可至 Insight 数据库内查看粒细胞集落刺激因子 (G-CSF) 是一种糖蛋白,可与粒系祖细胞或成熟中性粒细胞表面的特异性受体结合,促进粒系祖细胞的增殖分化以及增强中性粒细胞的吞噬和杀伤能力。该药是肿瘤化疗中最常用的辅助药物之一,也可以用于骨髓移植中造血干细胞的动员和移植后骨髓造血功能的重建,以及改善骨髓发育不良综合征或骨髓增生异常综合征等原因引起的中性粒细胞减少症状。
G-CSF 是国内外临床指南首推的放化疗相关中性粒细胞减少症药物,市场广阔。据 2019 年《柳叶刀肿瘤学》在线发表一项基于人口学的研究预测,2019 年全球肿瘤患者是 1,929 万人,至 2040 年全球肿瘤患者预计约 2,600 万人,其中中国预计会达到 625 万。
虽然如今癌症疗法正在不断迭代,化疗仍是重要治疗方案,针对化疗导致的中性粒细胞减少治疗需求庞大。G-CSF 包括短效和长效两种类型,前者在每个化疗周期内需要每日给药 1~2 次,而后者在一个化疗周期中往往只需给药 1 次。2020 年整体市场已有约 80.93 亿元规模,而长效市场占比正在加速扩大,由 2017 年的 9.99 亿元(25%)上升至 2020 年的 52.71 亿元(65%)。
除了本身拥有庞大市场需求之外,对于拥有丰富抗肿瘤管线和销售网络的国内大药企而言,长效升白药和企业自身管线能够形成良好协同。
全球首个长效 rhG-CSF 是安进开发的 Neulasta(培非格司亭),该产品上市第二年销售额就接近 Neupogen,成为安进的重磅药物,2016 年达到销售额峰值(47.15 亿美元),近三年来销售额虽然有所下降,但仍保持在 30 亿美元以上。
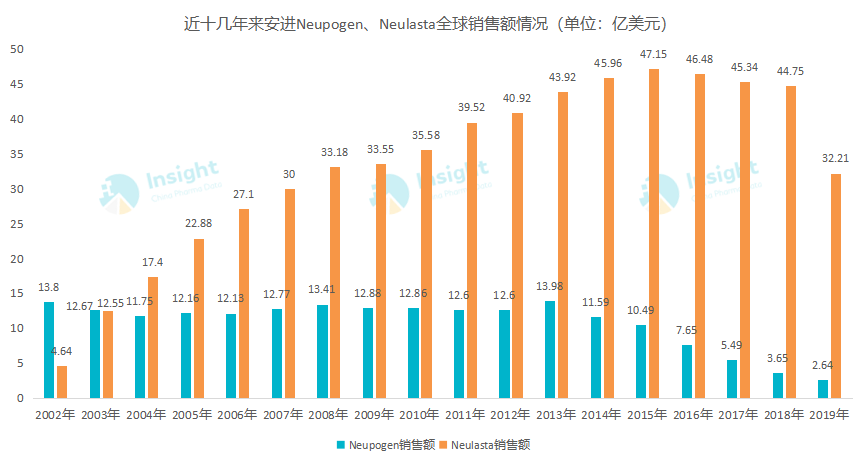
而在国内,国内共 4 款长效升白药获批上市,石药集团的津优力、齐鲁制药的新瑞白、恒瑞医药的艾多(简称 19K)和山东新时代的重组人粒细胞刺激因子。
【编辑:amanda】 国际药物制剂网 本文链接: http://www.phexcom.cn/hydt.aspx